吉林推薦的肺纖維化模型實驗外包
肺纖維化模型在醫學研究中扮演了至關重要的角色,它為我們深入理解肺纖維化在不同年齡和性別患者中的差異提供了有力幫助。這一模型能夠模擬出不同年齡和性別患者的生理特點,以及肺纖維化在這些特定人群中的獨特表現。通過對比不同組別的模型數據,研究人員能夠發現肺纖維化在不同年齡和性別患者中的病理變化差異,如細胞類型的差異、炎癥反應的強度等。這些發現有助于我們更準確地評估肺纖維化在特定人群中的風險,以及為制定個性化的治療方案提供科學依據。因此,肺纖維化模型在推動肺纖維化疾病的精細醫療方面具有重要作用。肺纖維化模型為研究肺纖維化的預防和早期干預提供了幫助。吉林推薦的肺纖維化模型實驗外包
肺纖維化模型是一種強大的工具,它通過精細地模擬不同因素引起的肺纖維化過程,為開發新的療愈方法提供了極大的幫助。這些因素可能包括環境污染、藥物副作用、遺傳因素以及特定的疾病過程等。通過構建這些復雜的模擬場景,研究人員能夠觀察到各種因素如何作用于肺部組織,觸發纖維化的產生和發展。這樣的模擬不僅有助于研究人員深入理解疾病背后的機制,還能夠評估不同療愈方法在模擬環境中的效果,從而篩選出具有潛力的療愈候選藥物或策略。這種科學的方法為肺纖維化的療愈研究帶來了更新性的進步,為改善患者的生活質量提供了希望。吉林推薦的肺纖維化模型實驗外包肺纖維化模型為研究疾病過程中的細胞代謝變化提供了幫助。
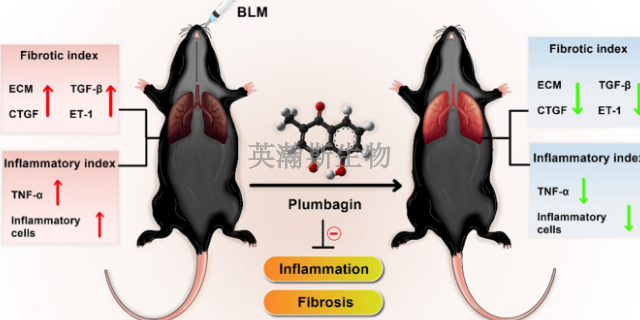
肺間質纖維化的形成是許多慢性肺疾病的共同結局,其病理特點是長期肺部炎癥導致肺泡持續性損傷以及細胞外基質(EcM)的反復破壞、修復和改建。博萊霉素引起的急性肺損傷(ALI)可導致成纖維細胞及肌成纖維細胞的增生,這些增生的細胞可產生大量ECM,比較終導致纖維化的形成。給予博萊霉素后小鼠表現為炎癥反應,早期為急性中性粒細胞浸潤,隨后過渡為淋巴細胞增多的慢性表現,與Izbicki等“的研究結果一致。Tarnell等的研究指出,纖維化模型BALF中中性粒細胞比血液中中性粒細胞產生更多的超氧陰離子。然而這種反應是暫時的,在明顯纖維化發生之前中性粒細胞就已恢復到正常水平,所以這些細胞可能并不直接作用于纖維化的起始。
除了急性損傷模型外,研究人員還開發了模擬環境或職業暴露導致的慢性肺纖維化模型,其中相當有代表性的是吸入性或灌注性二氧化硅(Silica)模型和吸入性石棉(Asbestos)模型。這些模型通過讓動物長期或一次性高劑量暴露于顆粒物,誘發矽肺病或石棉肺,這兩種疾病都是由顆粒物引發的慢性炎癥和持續性纖維化。二氧化硅顆粒被肺泡巨噬細胞吞噬后,會誘導巨噬細胞凋亡并釋放大量促炎癥和促纖維化細胞因子(如IL-1 $\beta$ 和TGF-$\beta 1$),從而啟動和維持纖維化過程。與博萊霉素模型相比,顆粒物誘導的模型具有更長的潛伏期和更慢的疾病進展速度,更貼近于人類慢性間質性肺病的自然病程,非常適合用于研究疾病的慢性演變過程以及長期干預策略的有效性。然而,這類模型的建模周期長(通常需要 $6$ 周至數月),且結果的異質性較大,對實驗操作和環境控制的要求更高。肺纖維化模型有助于理解肺纖維化在不同年齡和性別患者中的差異。
肺纖維化可能繼發于其他疾病。這些疾病中的大部分是間質性肺病,例如自身免疫性疾病、病毒***和細菌***(如結核病)。它們可能導致肺上葉或下葉的纖維化改變,以及肺部的其他微觀損傷。然而,肺纖維化也可能在缺乏任何已知病因的情況下出現,這被稱為“特發性”大多數特發***例被診斷為特發性肺纖維化。這是對稱為尋常型間質性肺炎(UIP)的一類組織病理學特征的排他性診斷。對于上述兩種情況,不斷有證據表明肺纖維化的發生存在遺傳傾向。例如研究發現,一些有肺纖維化病史的家庭存在表面活性劑蛋白C(SP-C)的突變。[9]15% 的肺纖維化患者存在編碼端粒酶的TERC或TERT基因的常染色體顯性突變肺纖維化模型揭示了疾病過程中炎癥介質的作用。寧夏比較好的肺纖維化模型有哪家
科學家通過肺纖維化模型發現了一些與疾病相關的微小RNA。吉林推薦的肺纖維化模型實驗外包
在肺纖維化模型的研究中,科學家們發現了一個關鍵的因素:肺纖維化的發展與氧化應激和抗氧化防御系統之間的失衡緊密相關。氧化應激是指機體內活性氧自由基的過量產生,而抗氧化防御系統則負責去除這些有害的自由基,保護細胞和組織免受損傷。在肺纖維化模型中,當肺部受到外界刺激或損傷時,氧化應激水平會明顯升高,而抗氧化防御系統的功能可能受損,導致兩者之間的平衡被打破。這種失衡狀態加劇了肺組織的氧化損傷,促進了肺纖維化的進展。因此,了解并調節氧化應激與抗氧化防御系統之間的平衡,對于預防和療愈肺纖維化具有重要意義。吉林推薦的肺纖維化模型實驗外包
- 云南真實的eae模型有哪家 2025-12-19
- 陜西真實的eae模型實驗外包 2025-12-19
- 浙江比較好的eae模型實驗外包 2025-12-19
- 遼寧靠譜的eae模型 2025-12-19
- 廣西靠譜的eae模型哪家口碑好 2025-12-19
- 福建真實的eae模型有哪些 2025-12-19
- 內蒙古真實的eae模型哪家口碑好 2025-12-19
- 山東專業的eae模型有哪家 2025-12-19
- 內蒙古專門做eae模型實驗外包 2025-12-19
- 福建大鼠eae模型是哪家 2025-12-19
- 海南哪里有醫用高分子夾板技術指導 2025-12-20
- 浦東新區聚甲醛誠信合作 2025-12-20
- 昆山瑞克式助聽器上門驗配 2025-12-20
- 成都輕便上臂假肢 2025-12-20
- 奉賢區運用實驗儀器專賣店 2025-12-20
- 崇明區作用實驗儀器市價 2025-12-20
- 稱量分離細胞培養皿 2025-12-20
- DNA植絨拭子批發廠 2025-12-20
- 1-溴-2-芐氧基乙烷報價 2025-12-20
- 上海隱形助聽器定制 2025-12-20