甘肅專業的eae模型如何構建
MOG,英文全名Myelinoligodendrocyteglycoprotein,中文名髓鞘少突膠質細胞糖蛋白,髓鞘的一種微量成分,屬于免疫球蛋白超家族成員之一。t也是特定表達于***系統(CNS)的自身抗原,誘導多發性硬化癥的原發性脫鞘特征。MOG(35-55)是髓鞘少突膠質細胞糖蛋白的免疫優勢表位,能夠誘導強烈的T細胞和B細胞應激反應,具高度致腦炎性,能夠誘導嚙齒類動物的實驗性白身免疫性腦脊髓炎(EAE)模型。EAE是**普遍的MS動物模型,具有MS許多的臨床和病理生理學特征。單次注射MOG(35-55)能夠產生一種復發-緩解型神經性疾病,表現出大量斑塊狀脫髓鞘病癥。1-甲基-4-苯基-1,.2,3,6-四氫吡啶(MPTP)誘導的多巴胺神經元損傷模型,免疫接種MOG(35-55)能抑制該神經元的白發再生功能。抗原誘導EAE模型后一般都在注射抗原佐劑乳化物后10d左右開始出現癥狀。甘肅專業的eae模型如何構建
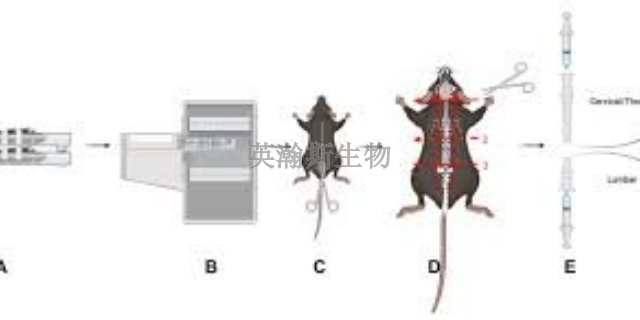
EAE動物模型的研究不僅為我們深入探索多發性硬化癥(MS)的發病機制提供了有力的工具,更在推動MS的臨床診斷和***技術方面發揮著舉足輕重的作用。通過對這一模型的深入研究,科學家們得以更***地了解MS的病理生理過程,從而為開發新的診斷方法提供了理論依據。同時,EAE動物模型也為評估新型***藥物的療效和安全性提供了重要的實驗平臺,為MS的臨床***提供了更為精細和個性化的方案。此外,隨著對EAE動物模型研究的不斷深入,我們有望在未來發現更多針對MS的有效***方法,為患者帶來更好的***效果和生活質量。因此,EAE動物模型的研究無疑將為MS的臨床診斷和***技術的進步注入新的動力。湖南比較好的eae模型是哪家與對照組相比,EAE模型組小鼠脊髓中活化的小膠質細胞數量增多。
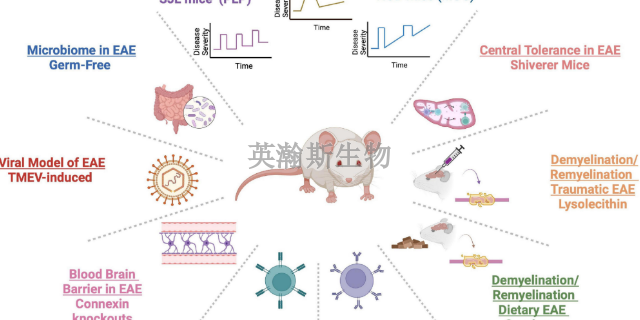
比較不同的神經功能損傷評分標準對小鼠實驗性自身免疫性腦脊髓炎(EAE)運動功能障礙評估的效能。方法:應用MOG35-55多肽加完全福氏佐劑乳化后免疫20只C57BL/6小鼠,復制EAE小鼠模型,并使用3種不同的評分標準(Kono's5分法、Hooper's7分法、Weaver's15分法)觀察和評估實驗動物的發病情況,對實驗小鼠在發病初期、高峰期的神經功能障礙進行定量的功能損傷評價。結果:3種評分標準比較,在發病初期,15分法和7分法評估神經損傷癥狀的敏感性相當,比5分法高;高峰期,以癥狀評分與病理評分的相關性程度來比較3種評分法的效度,15分法效度比較高,7分法次之。結論:Weaver's15分法評價EAE模型神經功能損傷癥狀,具有明顯的優勢,推薦作為今后EAE研究的優先評分法。
EAE模型的被動轉移實驗是研究其發病機制的**直接證據,也是研究EAE的***及預防措施的良好模型。將抗原***的PLP特異性T細胞轉輸給同一品系的正常大鼠或小鼠,也可引起EAE。MBP特異性自身反應性T細胞在MS的發病機制中也起著關鍵作用,T細胞必須先在外周活化,通過血管內皮細胞進入CNS才能致病。EAE的神經癥狀通常根據Kono等提出的標準分為5級。0級:無任何臨床癥狀;1級:動物尾巴無力,2級:尾部無力+肢體無力,3級:肢體輕度麻痹,4級:肢體嚴重麻痹,被動翻身后不能復原;5級:瀕死狀態或死亡。EAE具有復雜的神經藥理學特征,許多目前已用或即將使用的MS藥物得以開發、測試或驗證,基于EAE研究。
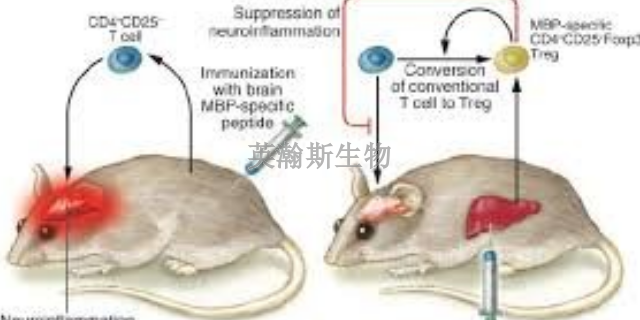
常用的致敏抗原有髓鞘堿性蛋白(MBP)或其多肽片斷(如MBP peptide 89—101)以及蛋白脂(PLP)等。長期以來MBP和PLP被認為是引起EAE和MS的主要抗原,MBP是髓鞘中抗原性比較強的蛋白質,占髓鞘總蛋白的40%,等電點在10以上,是強堿性蛋白質。研究表明MBP可***體內Th+細胞,使之穿過血腦屏障,攻擊自身神經髓鞘的MBP,從而導致***白質脫髓鞘,引起EAE模型或MS。近年來多用MBP肽代替MBP免疫動物。PLP是高度疏水的膜蛋白,對PLP不同肽決定簇發生反應的CD4+T細胞能誘導急性、慢性復發型及慢性進展型EAE。在MS患者體內也發現與PLP抗原決定簇發生反應的T細胞。 MOG是目前常用建立EAE模型的髓鞘抗原,多以誘發慢性EAE(Chronic EAE)模型。重慶真實的eae模型如何構建
eae模型是實驗性自身免疫性腦脊髓炎模型的縮寫。甘肅專業的eae模型如何構建
實驗性自身免疫性腦脊髓炎(EAE)是一種以特異性致敏的CD4+T細胞介導為主的,以***系統內小血管周圍出現單個核細胞浸潤及髓鞘脫失為特征的自身免疫性疾病,是人類多發性硬化(MS)的理想動物模型,在臨床神經免疫學的研究中具有重要意義。抗原佐劑為非特異性免疫增強劑,它可改變抗原的物理性狀,延長抗原在體內的儲留時間,刺激抗原提呈細胞及淋巴細胞,從而增強和擴大免疫應答效果,它還能引起遲發性血腦屏障通透性增加和自身免疫反應。甘肅專業的eae模型如何構建
- 云南真實的eae模型有哪家 2025-12-19
- 陜西真實的eae模型實驗外包 2025-12-19
- 浙江比較好的eae模型實驗外包 2025-12-19
- 遼寧靠譜的eae模型 2025-12-19
- 廣西靠譜的eae模型哪家口碑好 2025-12-19
- 福建真實的eae模型有哪些 2025-12-19
- 內蒙古真實的eae模型哪家口碑好 2025-12-19
- 山東專業的eae模型有哪家 2025-12-19
- 內蒙古專門做eae模型實驗外包 2025-12-19
- 福建大鼠eae模型是哪家 2025-12-19
- 佛山1470nm國產半導體激光治療儀廠家電話 2025-12-19
- 吳江區服務軟霧吸入器加盟連鎖店 2025-12-19
- 松江區定制吻合器工廠直銷 2025-12-19
- 深圳醫院智慧管理系統多少錢一套 2025-12-19
- 山西疫苗佐劑QS-21 2025-12-19
- 姑蘇區常見一次性注射器資費 2025-12-19
- 武漢本地活細胞成像分析系統直銷價格 2025-12-19
- 附近哪里有助腿器誠信合作 2025-12-19
- 銀杏葉片工廠 2025-12-19
- 珠海有實力的nmn定制廠家 2025-12-19