如何評定藥物的安全性
環境污染是NAFLD發生的重要危險因素。在動物實驗中,越來越多的證據表明高脂肪飲食(HFD)會加重環境化學物質引起的NAFLD。在過去的幾十年里,超重和肥胖已成為世界范圍內普遍存在的健康威脅,并與NAFLD風險的增加密切相關。在此,我們的目的是確定暴露于TBPH是否會誘導NAFLD進展及其潛在機制。斑馬魚作為模型生物,在肝臟細胞組成、功能、信號和介導肝臟疾病的細胞過程方面與人類相似,使其成為研究肝臟疾病基本機制的有用系統。斑馬魚被喂食正常飲食(ND)或HFD,并進行生化測試、組織病理學觀察和肝臟轉錄譜分析以評估NAFLD易感性。為了進一步探索NAFLD發病機制的潛在毒理學機制,我們研究了表觀遺傳修飾(例如DNA甲基化)。我們的研究結果表明,TBPH暴露破壞了斑馬魚的肝臟脂質代謝并誘發了NAFLD。斑馬魚模型評價半數致死濃度。如何評定藥物的安全性
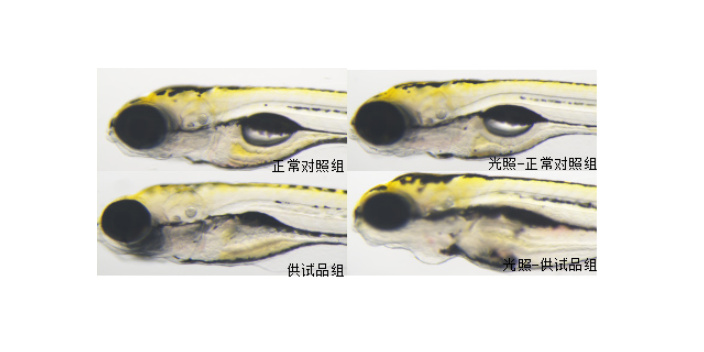
中藥口服后需經腸道菌群代謝才能發揮療效,這一過程被稱為“菌群-中藥互作”。以人參為例,其原型皂苷Rb?在腸道菌群作用下轉化為活性代謝物Rd和F?,后者對神經元的保護作用較原型增強5倍。通過宏基因組測序發現,擬桿菌門和厚壁菌門是主要代謝菌群,其產生的β-葡萄糖苷酶可水解皂苷糖基。實驗構建的“無菌小鼠+菌群移植”模型證實,移植人參代謝菌群的小鼠,其腦缺血損傷面積較普通小鼠減少40%。此外,菌群代謝產物(如短鏈脂肪酸)還可通過腸-腦軸調節免疫功能。這些發現為中藥“菌群依賴性療效”提供了機制解釋,也為個性化用藥提供了菌群檢測指標。中藥功效檢測利用斑馬魚模型評價軟骨修復功效。
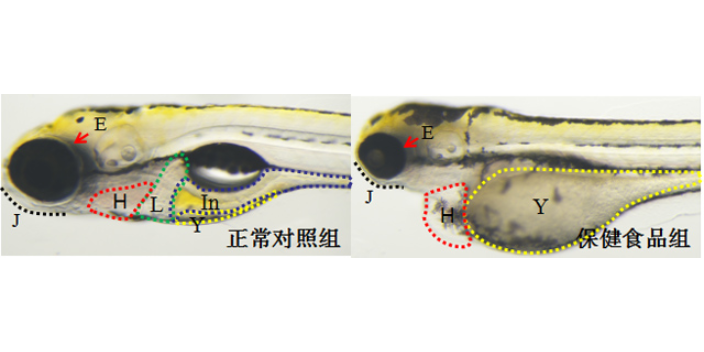
在科技日新月異的現在,人類對罕見病的研究與醫療不斷取得新的突破。肌萎縮側索硬化癥(Amyotrophiclateralsclerosis,ALS),作為一種目前仍無法痊愈的、具有臨床異質表現的多基因、多因素、進行性的神經退行性疾病,其特征是上、下行運動神經元丟失。斑馬魚,由于其與人類基因高度相似、胚胎透明、遺傳操作便利等特點,不僅可實現不同細胞的可視化從而觀察運動神經元或肌肉細胞的病變,而且可高通量檢測和分析運動相關的行為學改變,為探索ALS中運動障礙的病理機制、篩選新的潛在藥物、發現臨床新療法等提供了良好的工具,呈現出巨大的應用潛力。
隨著分子生物學技術的不斷發展,其在藥品機理研究中發揮著越來越重要的作用。基因編輯技術如CRISPR-Cas9的出現,使科研人員能夠精細地對細胞或動物模型的基因進行敲除、插入或修改,從而研究特定基因與藥物作用之間的關系。例如,通過敲除細胞中的某個基因,觀察藥物對細胞功能的影響是否改變,以此確定該基因是否為藥物作用的靶點或相關調控基因。蛋白質組學技術則可多方面分析藥物作用后細胞內蛋白質的變化情況,通過質譜技術鑒定蛋白質的種類、修飾狀態及表達量變化,幫助發現藥物作用的新靶點和潛在機制。此外,熒光標記技術能夠實時追蹤藥物在細胞內的運輸路徑、與靶點的結合過程,直觀地展現藥物發揮作用的動態過程。這些分子生物學技術從基因和蛋白質水平深入解析藥物作用機理,極大地推動了藥品機理研究的發展,為創新藥物研發提供了有力的技術支撐。利用斑馬魚模型評價降尿酸功效。
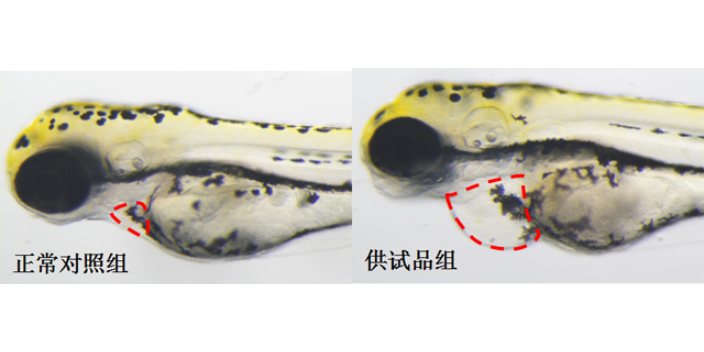
中藥對免疫系統的調節作用常涉及細胞因子網絡的動態平衡。以雷公藤甲素為例,其可通過抑制NF-κB通路,下調TNF-α、IL-6等促炎因子,同時上調IL-10、TGF-β等抑炎因子,緩解類風濕關節炎癥狀。實驗顯示,雷公藤甲素處理后的佐劑性關節炎大鼠,其關節腫脹度較對照組降低60%。另一機制是中藥對T細胞亞群的調節,如黃芪多糖可促進調節性T細胞(Treg)分化,抑制Th17細胞過度活化,維持免疫耐受。此外,中藥復方(如玉屏風散)可通過調節腸道菌群,影響短鏈脂肪酸(如丁酸)產生,間接調節免疫細胞功能。這些細胞因子網絡研究,為中藥免疫調節提供了系統生物學視角。藥品是什么,藥物是什么,你知道嗎?藥物藥效評價平臺
斑馬魚模型評價胚胎毒性。如何評定藥物的安全性
中藥活性成分的分離與鑒定是研究的第一步,依賴色譜、質譜等先進技術。高效液相色譜(HPLC)是分離中藥多組分的常用方法,通過調整流動相和固定相,可實現高分辨率分離。例如,利用反相HPLC從三七中分離出人參皂苷Rg1、Rb1等成分。質譜技術(如LC-MS/MS)則用于鑒定分子結構,通過碎片離子分析確定化合物類型。例如,通過高分辨質譜可快速識別黃芩中的黃芩苷、漢黃芩苷等黃酮類成分。此外,核磁共振(NMR)技術可進一步解析分子立體結構,為活性成分的合成或結構修飾提供基礎。這些技術的結合,使中藥復雜成分的解析效率大幅提升。如何評定藥物的安全性
- 斑馬魚技術資料多少錢 2025-12-20
- 甘肅做斑馬魚實驗的公司 2025-12-20
- 四川斑馬魚實驗的可靠性 2025-12-20
- 斑馬魚微視行為分析系統 2025-12-20
- 河南斑馬魚實驗 2025-12-20
- 斑馬魚實驗系統設備 2025-12-20
- 內蒙古斑馬魚實驗委托 2025-12-20
- 斑馬魚一站式服務報價 2025-12-20
- 斑馬魚基因研究公司 2025-12-20
- 甘肅斑馬魚實驗中心 2025-12-20
- 閔行區自動展示車加工信息中心 2025-12-20
- 瑤海區運營代理記賬報價 2025-12-20
- 虹口區比較好的企業形象策劃 2025-12-20
- 安徽外包直播策劃平臺 2025-12-20
- 寶山區咨詢保安服務服務熱線 2025-12-20
- 參考稅務服務是什么 2025-12-20
- 云南手機電子病歷系統(HIS系統)時代 2025-12-20
- 璧山區精細GEO生成式引擎優化推廣 2025-12-20
- 浙江常規品牌策劃推廣服務電話 2025-12-20
- 晉源區品牌辦公自動化軟件開發供應商家 2025-12-20