北京全人源單結(jié)構(gòu)域(VHH)合成文庫(kù)技術(shù)應(yīng)用
VHH 作為駱駝科動(dòng)物特有的單鏈抗體,具有分子量小(約 15kDa)、組織穿透性強(qiáng)、穩(wěn)定性高的特點(diǎn),在病毒中和、成像診斷等領(lǐng)域表現(xiàn)出獨(dú)特潛力。全人源 VHH 合成文庫(kù)將逐步替代部分傳統(tǒng)單克隆抗體,尤其在實(shí)體瘤、神經(jīng)疾病等領(lǐng)域憑借穿透性優(yōu)勢(shì)占據(jù)主導(dǎo)。同時(shí),其與基因治療、細(xì)胞治療的融合應(yīng)用(如作為 AAV 靶向配體)將加速遺傳病和罕見病治療的突破。此外,合成文庫(kù)結(jié)合高通量篩選的模式,可明顯降低中小企業(yè)的創(chuàng)新門檻,推動(dòng)生物制藥創(chuàng)新生態(tài)的民主化,使抗體研發(fā)從 “少數(shù)企業(yè)” 走向 “更廣的科研普惠”。上海溪長(zhǎng)生物的全人源單重鏈合成文庫(kù),應(yīng)用前景廣,抗體發(fā)現(xiàn)效率高。北京全人源單結(jié)構(gòu)域(VHH)合成文庫(kù)技術(shù)應(yīng)用
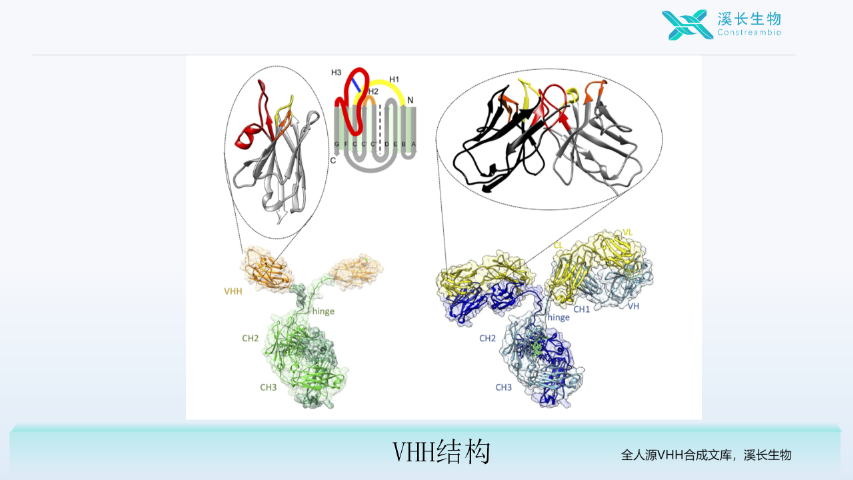
單域抗體指由抗體或新抗原受體單一可變結(jié)構(gòu)域構(gòu)成的具有抗原結(jié)合活性的基因工程抗體。由于其分子量小、穩(wěn)定性好和抗原親和力高的特點(diǎn),現(xiàn)已成為抗體工程領(lǐng)域的研究新熱點(diǎn)。到24年8月為止,全球約有30個(gè)單域抗體臨床項(xiàng)目正在開展中。同時(shí),該文庫(kù)支持定制化設(shè)計(jì),可根據(jù)具體需求與各種功能模塊進(jìn)行融合,構(gòu)建出滿足不同治療或診斷需求的多功能抗體。上海溪長(zhǎng)生物還提供多方位的技術(shù)支持和服務(wù),從文庫(kù)篩選到抗體優(yōu)化,專業(yè)團(tuán)隊(duì)全程保駕護(hù)航,助力客戶快速獲得理想的抗體分子,推動(dòng)抗體藥物研發(fā)項(xiàng)目順利進(jìn)展。北京全人源單結(jié)構(gòu)域(VHH)合成文庫(kù)技術(shù)應(yīng)用全人源 VHH 合成文庫(kù)選上海溪長(zhǎng),性價(jià)比更高,服務(wù)更周到。
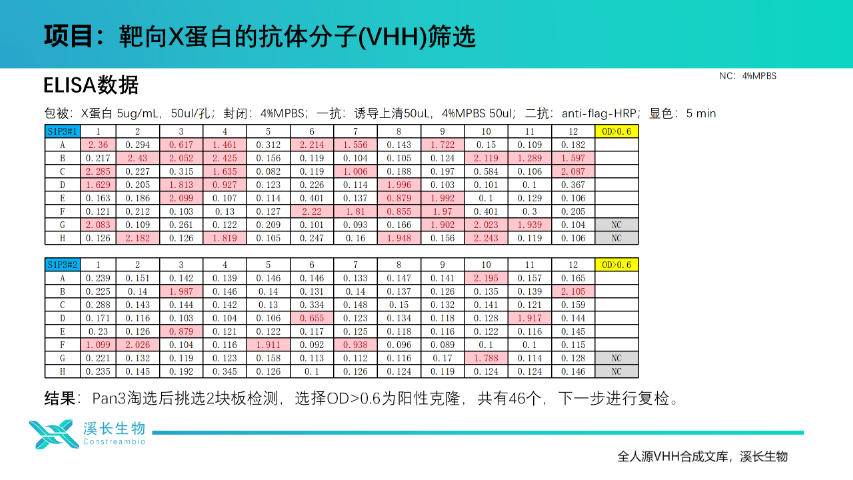
針對(duì)傳統(tǒng)平臺(tái)的技術(shù)瓶頸,全人源 VHH 合成文庫(kù)提供了更優(yōu)解決方案。例如,針對(duì)免疫原性導(dǎo)致的臨床失敗問(wèn)題,VHH 憑借全人源序列直接進(jìn)入臨床,無(wú)需耗時(shí)改造;對(duì)于實(shí)體瘤藥物遞送效率低的難題,VHH 的小分子量使其天然具備穿透優(yōu)勢(shì),無(wú)需聯(lián)合基質(zhì)降解酶(避免增加毒性風(fēng)險(xiǎn));在難成藥靶點(diǎn)篩選方面,VHH 合成文庫(kù)通過(guò)預(yù)優(yōu)化 CDR-H3 直接針對(duì)靶點(diǎn)表位設(shè)計(jì),替代了傳統(tǒng)依賴動(dòng)物免疫的高成本模式(如轉(zhuǎn)基因小鼠成本超 10 萬(wàn)美元);在雙特異性抗體構(gòu)建上,VHH 單鏈串聯(lián)雙結(jié)構(gòu)域的產(chǎn)率可達(dá) 70% 以上,遠(yuǎn)高于傳統(tǒng)肽鏈重組或化學(xué)偶聯(lián)的不足 30% 產(chǎn)率;在生產(chǎn)成本方面,VHH 的原核表達(dá)系統(tǒng)使小規(guī)模生產(chǎn)成為可能,成本較傳統(tǒng)真核表達(dá)降低 90%。
從科研到臨床,溪長(zhǎng)生物加速創(chuàng)新藥上市進(jìn)程;溪長(zhǎng)生物全人源VHH合成文庫(kù)通過(guò)優(yōu)化CDR3區(qū)氨基酸組合,提升抗體熱穩(wěn)定性與pH耐受性,候選分子在45℃條件下仍保持80%以上活性。平臺(tái)支持多輪親和力成熟迭代,親和力提升達(dá)1000倍以上。目前,基于全人源單結(jié)構(gòu)域VHH合成文庫(kù)開發(fā)的多個(gè)納米抗體藥物已進(jìn)入臨床前研究,有望成為治療實(shí)體瘤、自身免疫疾病的新一代重磅藥物。上海溪長(zhǎng)生物全人源VHH合成文庫(kù),助力醫(yī)藥行業(yè)實(shí)現(xiàn)國(guó)產(chǎn)化,提高產(chǎn)品的可及性。我們的文庫(kù)為制藥和診斷行業(yè)提供了豐富的候選抗體資源,推動(dòng)行業(yè)的快速發(fā)展。探索 VHH 抗體領(lǐng)域,上海溪長(zhǎng)全人源單重鏈合成文庫(kù),豐富資源等你來(lái)。
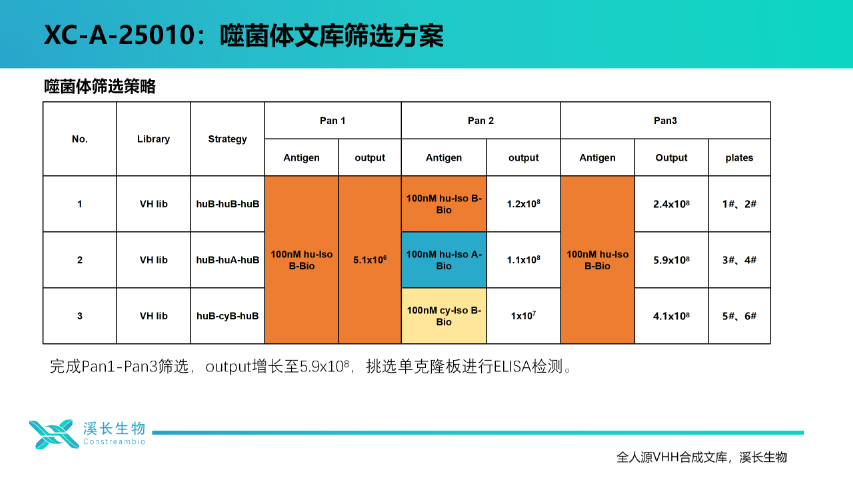
產(chǎn)學(xué)研深度融合,溪長(zhǎng)生物打造抗體開發(fā)"中國(guó)方案",溪長(zhǎng)生物聯(lián)合上海交大、復(fù)旦大學(xué)等科研機(jī)構(gòu),構(gòu)建"基礎(chǔ)研究-技術(shù)開發(fā)-產(chǎn)業(yè)轉(zhuǎn)化"創(chuàng)新鏈條。全人源VHH合成文庫(kù)作為關(guān)鍵技術(shù)載體,合作開發(fā)不同靶點(diǎn)抗體分子。開展靶點(diǎn)驗(yàn)證與抗體初篩;技術(shù)開發(fā)階段,雙方聯(lián)合優(yōu)化篩選策略,達(dá)成合作共贏的一致共識(shí)。在篩選的同時(shí)提供抗體優(yōu)化的專業(yè)指導(dǎo),全程助力科研人員快速獲得高特異性、高親和力的 VHH 抗體,加速抗體藥物從實(shí)驗(yàn)室走向臨床的步伐。上海溪長(zhǎng)生物全人源單結(jié)構(gòu)域(VHH)合成庫(kù),人源框架設(shè)計(jì),免疫原性更低,成藥更安心!北京全人源單結(jié)構(gòu)域(VHH)合成文庫(kù)技術(shù)應(yīng)用
選擇上海溪長(zhǎng)全人源合成文庫(kù),讓VHH抗體篩選更簡(jiǎn)單 —— 你的科研加速引擎,就在這里!北京全人源單結(jié)構(gòu)域(VHH)合成文庫(kù)技術(shù)應(yīng)用
截至2023年7月,全球至少已有4款納米抗體藥物獲批上市。Ablynx公司研發(fā)的Caplacizumab(商品名為Cablivi?)納米抗體藥物,用于治療獲得性血栓性血小板減少性紫癜(aTTP)的成人患者,已于2018年8月31日獲歐洲藥物管理局(EMA)批準(zhǔn)上市,后于2019年2月6日獲美國(guó)食品藥品監(jiān)督管理局(FDA)批準(zhǔn)上市。傳奇生物的CAR-T細(xì)胞產(chǎn)品——西達(dá)基奧侖賽(CARVYKTI,英文通用名Ciltacabtagene Autoleucel)采用了獨(dú)特的二價(jià)納米抗體設(shè)計(jì),是FDA批準(zhǔn)的基于VHH的CAR-T產(chǎn)品,用于治療復(fù)發(fā)或難治性多發(fā)性骨髓瘤。Ablynx公司開發(fā)的另一款納米抗體藥物Ozoralizumab是人源化、三價(jià)的雙特異性納米抗體,由兩個(gè)抗人TNFα納米抗體和一個(gè)抗人血清白蛋白 (HSA) 納米抗體組成,已于2022年9月26日在日本獲批上市。康寧杰瑞研發(fā)的Envafolimab屬于PD-L1單域抗體Fc融合蛋白,已于2021年11月在中國(guó)上市。另外,目前有20多項(xiàng)納米抗體相關(guān)藥物進(jìn)入到臨床階段。北京全人源單結(jié)構(gòu)域(VHH)合成文庫(kù)技術(shù)應(yīng)用
- 湖南全人源單結(jié)構(gòu)域(VHH)合成文庫(kù)高性價(jià)比 2025-12-24
- 黑龍江全人源Fab合成噬菌體文庫(kù)方案 2025-12-23
- 貴州全人源單結(jié)構(gòu)域(VHH)合成文庫(kù)篩選時(shí)間 2025-12-23
- 湖北單結(jié)構(gòu)域文庫(kù)技術(shù)科普 2025-12-23
- 吉林VHH合成文庫(kù)流程 2025-12-23
- 上海溪長(zhǎng)全人源單結(jié)構(gòu)域(VHH)合成文庫(kù)方案 2025-12-23
- 河北全人源單重鏈合成文庫(kù)優(yōu)勢(shì) 2025-12-23
- 陜西全人源單重鏈合成文庫(kù)技術(shù)應(yīng)用 2025-12-23
- 吉林全人源單結(jié)構(gòu)域(VHH)合成文庫(kù)開發(fā)方案 2025-12-23
- 黑龍江合成噬菌體文庫(kù)流程解析 2025-12-23
- 陜西進(jìn)口成型片廠家 2025-12-24
- 楊浦區(qū)聚醚醚酮成本價(jià) 2025-12-24
- 河北中鼻拭子供應(yīng)商 2025-12-24
- 臺(tái)州醫(yī)用壓縮式霧化器口碑推薦 2025-12-24
- 杭州萊文Level臨床決策支持系統(tǒng)優(yōu)點(diǎn) 2025-12-24
- 南通定制植物冠層光合氣體交換測(cè)量系統(tǒng) 2025-12-24
- 普陀區(qū)皮膚科單機(jī)交互性能穩(wěn)定 2025-12-24
- 鹽田區(qū)標(biāo)準(zhǔn)生物試劑工廠直銷 2025-12-24
- 蘇州推薦洗鼻器工廠直銷 2025-12-24
- 陜西啟達(dá)醫(yī)療壓縮式霧化器價(jià)格-圖片-排行 2025-12-24