北京VHH合成文庫技術(shù)進展
對于科研人員和藥企而言,上海溪長生物的全人源VHH合成文庫是抗疫發(fā)現(xiàn)的高效率平臺。該文庫全人源的設計理念貫穿始終,抗體基因完全來自人類,徹底消除了免疫原性風險,為抗體藥物的臨床應用奠定了堅實的安全基礎。文庫構(gòu)建采用了前沿的技術(shù)手段,實現(xiàn)了高度的多樣性,能夠針對不同的靶點生成大量具有獨特結(jié)合特性的抗體。其中,VHH抗體的小分子量優(yōu)勢盡顯,其能夠輕松穿透實體瘤組織,有效解決了傳統(tǒng)抗體在病癥治療中難以深入病灶的難題,為實體瘤的靶向治療帶來新希望。上海溪長全人源 VHH 合成文庫,助力科研人員開啟抗體篩選之旅。北京VHH合成文庫技術(shù)進展
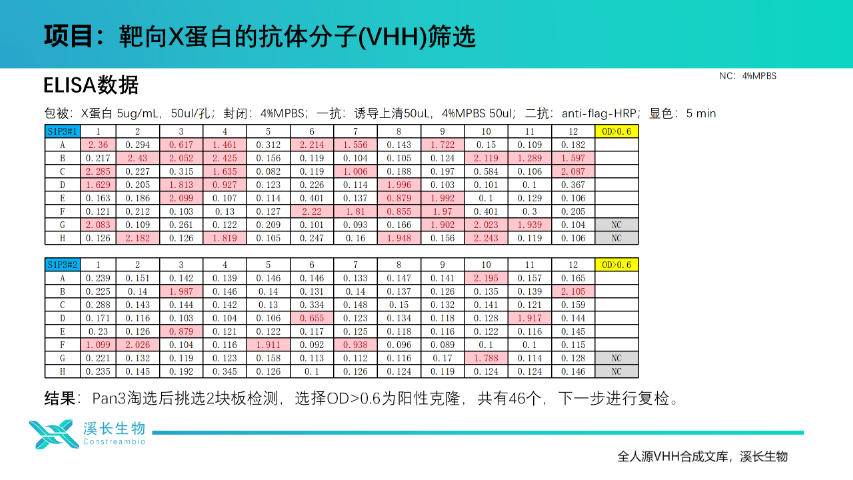
截至2023年7月,全球至少已有4款納米抗體藥物獲批上市。Ablynx公司研發(fā)的Caplacizumab(商品名為Cablivi?)納米抗體藥物,用于治療獲得性血栓性血小板減少性紫癜(aTTP)的成人患者,已于2018年8月31日獲歐洲藥物管理局(EMA)批準上市,后于2019年2月6日獲美國食品藥品監(jiān)督管理局(FDA)批準上市。傳奇生物的CAR-T細胞產(chǎn)品——西達基奧侖賽(CARVYKTI,英文通用名CiltacabtageneAutoleucel)采用了獨特的二價納米抗體設計,是FDA批準的基于VHH的CAR-T產(chǎn)品,用于治療復發(fā)或難治性多發(fā)性骨髓瘤。Ablynx公司開發(fā)的另一款納米抗體藥物Ozoralizumab是人源化、三價的雙特異性納米抗體,由兩個抗人TNFα納米抗體和一個抗人血清白蛋白(HSA)納米抗體組成,已于2022年9月26日在日本獲批上市。康寧杰瑞研發(fā)的Envafolimab屬于PD-L1單域抗體Fc融合蛋白,已于2021年11月在中國上市。另外,目前有20多項納米抗體相關(guān)藥物進入到臨床階段。北京VHH合成文庫技術(shù)進展上海溪長全人源 VHH 合成文庫,海量數(shù)據(jù),為抗體篩選開拓道路。

上海溪長生物憑借深厚的生物制藥經(jīng)驗與前沿技術(shù),打造全人源VHH合成文庫,為抗體發(fā)現(xiàn)領(lǐng)域注入新活力。該文庫匯聚高度多樣性抗體序列,通過噬菌體展示技術(shù),實現(xiàn)快速、準確高效篩選,為制藥和診斷行業(yè)提供高親和力、高特異性的候選抗體。文庫的構(gòu)建不僅體現(xiàn)了溪長生物在抗體人源化、改造方面的專業(yè)技術(shù),更彰顯了公司推動國內(nèi)醫(yī)藥行業(yè)自主創(chuàng)新和產(chǎn)業(yè)升級的決心。選擇溪長生物,就是選擇高效、可靠的抗體發(fā)現(xiàn)解決方案,共同開啟抗體發(fā)現(xiàn)的新紀元。
上海溪長生物提供從抗原設計到抗體表達與純化的一站式服務,讓您在抗體發(fā)現(xiàn)過程中省心省力。我們的專業(yè)團隊將全程參與您的項目,提供技術(shù)支持和咨詢服務,確保項目的順利進行。選擇溪長生物,就是選擇了一個能夠為您提供多方位、一站式服務的合作伙伴。海溪長生物全人源VHH合成文庫,以專業(yè)的技術(shù)服務和豐富的經(jīng)驗,贏得了客戶的認可和信賴。我們期待與您攜手合作,共同推動抗體發(fā)現(xiàn)領(lǐng)域的發(fā)展,共創(chuàng)輝煌未來。選擇溪長生物,就是選擇了一個能夠與您并肩作戰(zhàn)、共同成長的合作伙伴。上海溪長全人源 VHH 合成文庫,適配雙抗 / 多抗開發(fā),分子設計更靈活!
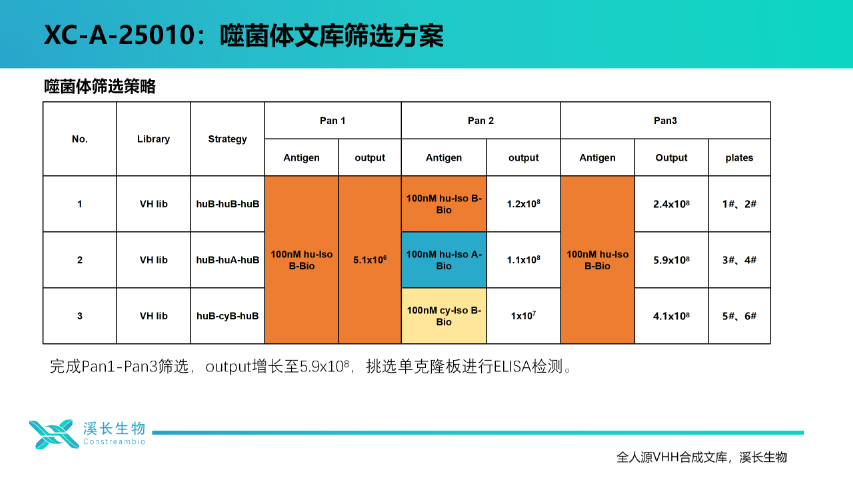
上海溪長生物全人源單結(jié)構(gòu)域VHH合成文庫,依托前沿噬菌體展示技術(shù),構(gòu)建起一個高度多樣的抗體資源庫。該文庫能通過高效篩選機制,快速鎖定高親和力、高特異性的候選抗體,為抗體藥物研發(fā)按下“加速鍵”。我們深知,在抗體研發(fā)的征途上,時間就是效率,質(zhì)量就是生命。因此,溪長生物致力于高效的服務,助力每一位合作伙伴在抗體研發(fā)領(lǐng)域搶占先機,共同開啟抗體研發(fā)的新篇章。如果您有新項目抗體開發(fā)需求,歡迎選擇上海溪長生物,我們一定給您滿意的交付,期待合作。上海溪長生物全人源單結(jié)構(gòu)域(VHH)合成庫,人源框架設計,免疫原性更低,成藥更安心!北京VHH合成文庫技術(shù)進展
上海溪長全人源VHH合成文庫,定制化建庫服務,適配稀缺靶點開發(fā)需求!北京VHH合成文庫技術(shù)進展
全人源VHH合成文庫在分子特性方面,完成了從小分子到大功能的突破;全人源VHH合成文庫產(chǎn)生的抗體分子量約15kDa,為單域結(jié)構(gòu),相比傳統(tǒng)IgG(~150kDa)或scFv(~25kDa),具有更強的組織穿透能力,在實體瘤中的穿透效率提升3倍,且能跨越血腦屏障,適合開發(fā)針對神經(jīng)性系統(tǒng)疾病的藥物。其結(jié)構(gòu)穩(wěn)定性也明顯更優(yōu),可耐受極端pH環(huán)境(3-11)和蛋白酶降解,無需冷鏈運輸。此外,VHH可直接通過基因工程融合熒光標記或其他功能域,便捷構(gòu)建雙特異性分子,而傳統(tǒng)抗體(如IgG)進行類似改造時需復雜操作,融合效率較低。北京VHH合成文庫技術(shù)進展
- 黑龍江全人源Fab合成噬菌體文庫方案 2025-12-23
- 貴州全人源單結(jié)構(gòu)域(VHH)合成文庫篩選時間 2025-12-23
- 湖北單結(jié)構(gòu)域文庫技術(shù)科普 2025-12-23
- 吉林VHH合成文庫流程 2025-12-23
- 上海溪長全人源單結(jié)構(gòu)域(VHH)合成文庫方案 2025-12-23
- 河北全人源單重鏈合成文庫優(yōu)勢 2025-12-23
- 陜西全人源單重鏈合成文庫技術(shù)應用 2025-12-23
- 吉林全人源單結(jié)構(gòu)域(VHH)合成文庫開發(fā)方案 2025-12-23
- 黑龍江合成噬菌體文庫流程解析 2025-12-23
- 中國香港合成文庫技術(shù)分享 2025-12-23
- 陜西進口成型片廠家 2025-12-24
- 楊浦區(qū)聚醚醚酮成本價 2025-12-24
- 河北中鼻拭子供應商 2025-12-24
- 臺州醫(yī)用壓縮式霧化器口碑推薦 2025-12-24
- 杭州萊文Level臨床決策支持系統(tǒng)優(yōu)點 2025-12-24
- 南通定制植物冠層光合氣體交換測量系統(tǒng) 2025-12-24
- 普陀區(qū)皮膚科單機交互性能穩(wěn)定 2025-12-24
- 鹽田區(qū)標準生物試劑工廠直銷 2025-12-24
- 蘇州推薦洗鼻器工廠直銷 2025-12-24
- 陜西啟達醫(yī)療壓縮式霧化器價格-圖片-排行 2025-12-24