河北單結構域文庫高性價比
VHH合成文庫是基于駱駝科動物重鏈抗體可變區(qū)(VHH)的基因工程技術平臺,通過人工設計和構建高度多樣化的抗體庫,實現(xiàn)高親和力、低免疫原性抗體的快速篩選。而上海溪長生物技術有限公司的全人源單結構域VHH合成文庫憑借其多樣性、人源化優(yōu)勢及高效篩選能力,已成為抗體藥物研發(fā)的重要工具。未來,隨著AI設計、高通量篩選和生產工藝優(yōu)化的深度融合,全人源VHH合成文庫將在自免、傳染病等領域持續(xù)突破,推動抗體藥物升級,歡迎項目咨詢交流。上海溪長全人源 VHH 合成文庫,適配雙特異性 VHH 開發(fā),一鍵串聯(lián)抗原結合域,多功能分子設計更靈活!河北單結構域文庫高性價比
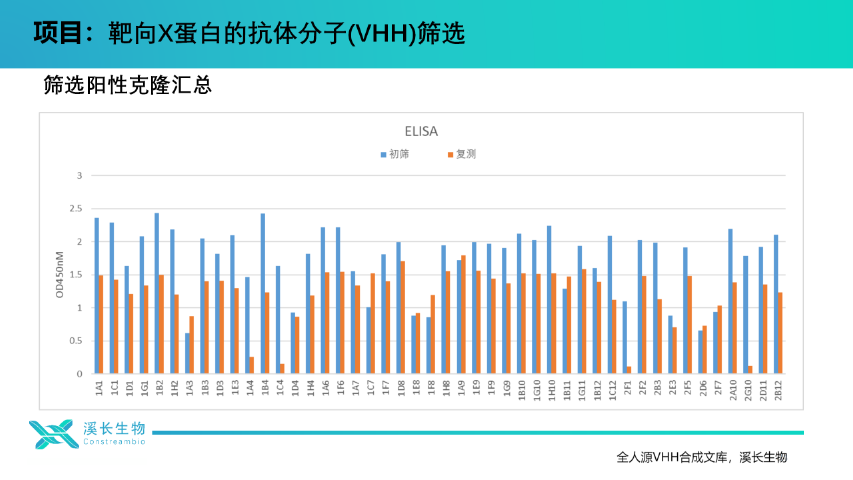
在抗體研發(fā)領域,全人源單結構域VHH合成文庫正成為創(chuàng)新突破的關鍵利器。相較于傳統(tǒng)抗體文庫,全人源單結構域VHH合成文庫具備獨特優(yōu)勢。其基于全人源序列設計,有效降低免疫原性風險,適配臨床治療性抗體開發(fā)需求。單結構域VHH分子量小、結構簡單,可穿透深層組織,結合特殊抗原表位,在自身免疫病等疾病靶點探索中,能挖掘常規(guī)抗體難以觸及的結合位點。文庫構建依托先進基因合成與篩選技術,涵蓋豐富序列多樣性,可快速篩選高親和力、高特異性VHH分子。無論是藥物研發(fā)企業(yè)加速抗體藥物管線推進,還是科研團隊開展前沿抗體機制研究,溪長生物的全人源單結構域VHH合成文庫助力突破研發(fā)瓶頸,開啟抗體設計與高效篩選的全新篇章,為生物醫(yī)藥創(chuàng)新發(fā)展注入強勁動力。上海單結構域文庫周期上海溪長全人源VHH合成文庫,多源整合,為抗體研究提供可靠支撐。
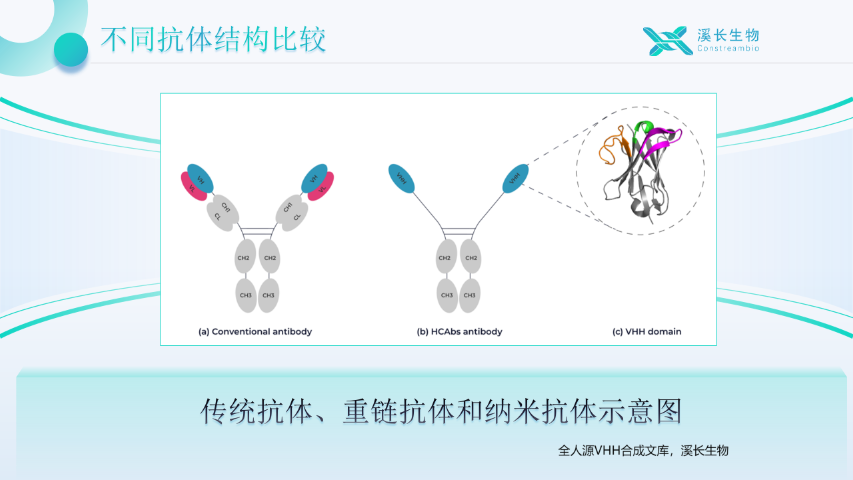
全人源VHH合成文庫將生產成本從“高門檻”到“普惠化”,該文庫的抗體可通過大腸桿菌或酵母等原核表達系統(tǒng)生產,從克隆到純化需10天,生產成本較傳統(tǒng)真核表達系統(tǒng)(如CHO細胞表達IgG)降低50%-80%,尤其適合小規(guī)模生產需求。例如,某VHH-偶聯(lián)物的生產成本為同類IgG-ADC藥物的1/3,且10L規(guī)模生產即可滿足科研或獸用需求。而傳統(tǒng)IgG類抗體依賴CHO細胞或HEK293等真核表達系統(tǒng),培養(yǎng)基和純化成本高昂,生產規(guī)模需100L起,對中小企業(yè)而言經濟壓力較大,但是全人源VHH合成文庫相比之下性價比就會高很多。
截至2023年7月,全球至少已有4款納米抗體藥物獲批上市。Ablynx公司研發(fā)的Caplacizumab(商品名為Cablivi?)納米抗體藥物,用于治療獲得性血栓性血小板減少性紫癜(aTTP)的成人患者,已于2018年8月31日獲歐洲藥物管理局(EMA)批準上市,后于2019年2月6日獲美國食品藥品監(jiān)督管理局(FDA)批準上市。傳奇生物的CAR-T細胞產品——西達基奧侖賽(CARVYKTI,英文通用名CiltacabtageneAutoleucel)采用了獨特的二價納米抗體設計,是FDA批準的基于VHH的CAR-T產品,用于治療復發(fā)或難治性多發(fā)性骨髓瘤。Ablynx公司開發(fā)的另一款納米抗體藥物Ozoralizumab是人源化、三價的雙特異性納米抗體,由兩個抗人TNFα納米抗體和一個抗人血清白蛋白(HSA)納米抗體組成,已于2022年9月26日在日本獲批上市。康寧杰瑞研發(fā)的Envafolimab屬于PD-L1單域抗體Fc融合蛋白,已于2021年11月在中國上市。另外,目前有20多項納米抗體相關藥物進入到臨床階段。上海溪長生物的全人源單重鏈合成文庫,應用前景廣,抗體發(fā)現(xiàn)效率高。
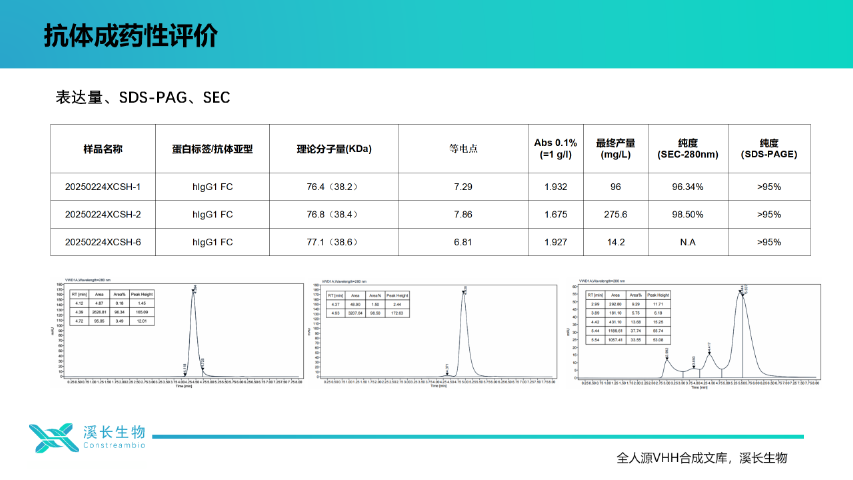
面對進口抗體試劑的市場壟斷,溪長生物全人源VHH合成文庫以自主知識產權技術打破技術封鎖。文庫采用全合成策略,避免動物免疫依賴,提升抗體開發(fā)效率與成功率。平臺支持診斷試劑、生物試劑關鍵原料開發(fā),已實現(xiàn)多款產品的國產替代,助力生物醫(yī)藥行業(yè)降本增效,推動產業(yè)鏈自主可控。溪長生物打造的全人源VHH合成文庫,庫容突破千億級,覆蓋多樣化表位空間,可準確匹配GPCR、離子通道等"不可成藥"靶點。通過噬菌體展示與核糖體展示技術融合,實現(xiàn)單輪篩選效率提升3倍,陽性克隆率高達90%以上。文庫支持多表位、多價性納米抗體開發(fā),滿足雙抗、ADC等新型藥物研發(fā)需求,為全球藥企提供"一站式"抗體發(fā)現(xiàn)解決方案。全人源 VHH 合成文庫選上海溪長,透明化服務流程,每一步都清晰可查!上海單結構域文庫周期
上海溪長生物全人源單結構域(VHH)合成庫,人源框架設計,免疫原性更低,成藥更安心!河北單結構域文庫高性價比
上海溪長生物全人源VHH合成文庫篩選效率相較傳統(tǒng)篩選路徑大幅提高,全人源VHH合成文庫的庫容量超過109,CDR-H3區(qū)域隨機化深度達15aa,結合AI預測技術預篩選高潛力克隆,可將篩選周期縮短至7-14天,且獲得的抗體平均親和力KD<1nM,部分可達pM級(如0.8pM)。對于膜蛋白(如GPCR)、淀粉樣蛋白等難成藥靶點,文庫通過預優(yōu)化CDR-H3設計,可直接針對靶點表位高效篩選。相比之下,傳統(tǒng)雜交瘤技術能產生<103個克隆,天然噬菌體文庫庫容量約10?-10?,篩選周期長達2-3周,且對難成藥靶點需依賴經驗性篩選,漏篩風險較高,獲得抗體的親和力通常在10nM級別河北單結構域文庫高性價比
- 黑龍江全人源Fab合成噬菌體文庫方案 2025-12-23
- 貴州全人源單結構域(VHH)合成文庫篩選時間 2025-12-23
- 湖北單結構域文庫技術科普 2025-12-23
- 吉林VHH合成文庫流程 2025-12-23
- 上海溪長全人源單結構域(VHH)合成文庫方案 2025-12-23
- 河北全人源單重鏈合成文庫優(yōu)勢 2025-12-23
- 陜西全人源單重鏈合成文庫技術應用 2025-12-23
- 吉林全人源單結構域(VHH)合成文庫開發(fā)方案 2025-12-23
- 黑龍江合成噬菌體文庫流程解析 2025-12-23
- 中國香港合成文庫技術分享 2025-12-23
- 普陀區(qū)皮膚科單機交互性能穩(wěn)定 2025-12-24
- 蘇州推薦洗鼻器工廠直銷 2025-12-24
- 陜西啟達醫(yī)療壓縮式霧化器價格-圖片-排行 2025-12-24
- 徐匯區(qū)比較好的實驗儀器現(xiàn)價 2025-12-24
- 福建哪個公司品類多美容院拓客工具 2025-12-24
- 貴州哪些活性益生菌有哪些 2025-12-24
- 江門兒童成長基因檢測公司 2025-12-24
- 萊文HIS 2025-12-24
- 無錫青少年脊柱側彎支具價格可以優(yōu)惠嗎 2025-12-24
- 山西植物提取QS-21 2025-12-24