北京抗體藥物熱原檢測MAT法
來源:
發(fā)布時間:2025-10-09
PBMC(外周血單個核細胞)用于 MAT 熱原檢測時,存在異質(zhì)性與血源供應兩大關鍵問題。從異質(zhì)性來看,PBMC 含 12% 單核細胞與 88% 淋巴細胞,且來自不同供體,細胞組成、功能狀態(tài)及熱原反應存在明顯差異,導致熱原刺激后 IL-6 釋放量波動大,標準化難度高。血源供應方面,除受獻血者數(shù)量、時間及采集血液政策限制外,EP2.6.30 還要求嚴格檢測乙肝、丙肝等標志物,且采集血液、處理、試劑制備全程需無菌操作,流程環(huán)節(jié)多、復雜度高,遠不及單核細胞系制備簡便,易影響熱原檢測的時效性與穩(wěn)定性。家兔法是熱原檢測 “金標準”,但操作繁瑣、耗時且需動物設施,存在明顯局限。北京抗體藥物熱原檢測MAT法
MAT 法熱原檢測標曲采用非倍比稀釋,而非 1-0.5-0.25 的倍比稀釋,主要優(yōu)勢在于提升標曲準確性與適用性,避免稀釋誤差影響。一是可密集覆蓋關鍵濃度區(qū)間:熱原檢測的重點關注區(qū)為低濃度拐點(如 0.0125-0.1EU/mL)與高濃度平臺區(qū)(如 0.5-1EU/mL),非倍比稀釋可在這些區(qū)間設置更多濃度點(如 0.0125、0.025、0.05、0.1、0.25、0.5、1EU/mL),提升曲線擬合精度,而倍比稀釋低濃度點少,易導致低濃度熱原定量不準。二是降低稀釋誤差累積:倍比稀釋需連續(xù)稀釋(如 1EU/mL→0.5EU/mL→0.25EU/mL),每一步誤差會累積,導致低濃度點實際濃度偏離理論值;非倍比稀釋通過單獨配制每個濃度點(如直接用標準品配制 0.025EU/mL),避免誤差累積,提升標曲可靠性。三是適配不同樣品濃度:非倍比稀釋可根據(jù)樣品預期濃度調(diào)整標曲范圍,如樣品預期濃度 0.05EU/mL,可增加 0.025、0.05、0.1EU/mL 點,確保樣品濃度落在標曲線性區(qū),而倍比稀釋范圍固定,靈活性差。這些優(yōu)勢使非倍比稀釋成為 MAT 法標曲配制的優(yōu)先選擇方式。
化學制藥熱原檢測家兔法替代方案湖州申科熱原檢測試劑盒中單核細胞系表面有多種Toll樣受體,可響應革蘭氏陽性菌、病毒等熱原。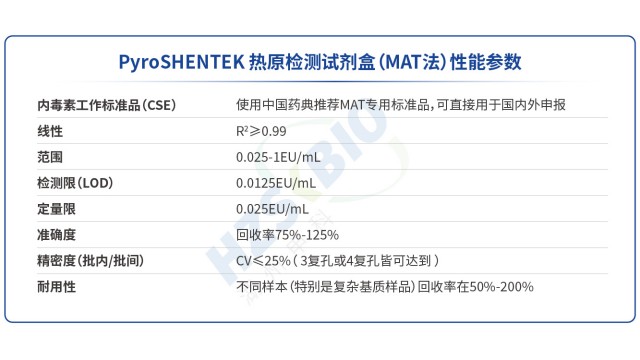
熱原是能引發(fā)恒溫動物體溫異常升高的物質(zhì)總稱,主要成分為細菌內(nèi)毒素(革蘭氏陰性菌脂多糖 LPS),同時涵蓋病毒、真菌毒素、支原體等非內(nèi)毒素熱原,其檢測是保障藥品與醫(yī)療器械安全性的關鍵環(huán)節(jié)。當前熱原檢測已形成 “特異性檢測 + 廣譜篩查” 互補的完整體系:以鱟試驗法(含天然 LAL 與重組 rCR/rFC 試劑)作為細菌內(nèi)毒素的特異性檢測手段,憑借 fg 級靈敏度成為制藥行業(yè)常規(guī)質(zhì)控方法,可通過凝膠法實現(xiàn)定性、動態(tài)濁度 / 顯色法完成定量;以家兔熱原試驗作為傳統(tǒng)廣譜篩查方法,雖操作繁瑣(需預試篩選基礎體溫穩(wěn)定家兔,正式試驗觀察 3 小時體溫變化),但仍是放射性質(zhì)的藥物、血液制品等高風險產(chǎn)品排除非內(nèi)毒素熱原的補充手段;以單核細胞活化反應測定(MAT)作為新興全熱原檢測技術,利用人源單核細胞(如 THP-1 細胞)釋放 IL-6、TNF-α 等細胞因子的特性,可同時識別內(nèi)毒素與非內(nèi)毒素熱原,契合疫苗、基因治療產(chǎn)品等對風險控制的需求。三種方法協(xié)同應用,從原料入廠到成品放行構建全流程熱原防控網(wǎng)絡,既保證對內(nèi)毒素的準確監(jiān)控,又避免非內(nèi)毒素熱原的遺漏風險。
在單核細胞活化試驗(MAT)的熱原檢測中,IL-6 被確定為關鍵檢測指標,而非 IL-1β 或 TNF-α,主要源于其在穩(wěn)定性、生物學關聯(lián)性及商業(yè)化應用上的優(yōu)勢。從穩(wěn)定性來看,IL-6 在體外培養(yǎng)環(huán)境中受個體免疫狀態(tài)影響較小,半衰期更長,實驗重復性更優(yōu),且檢測靈敏度高,能準確定量熱原污染水平;而 TNF-α 和 IL-1β 產(chǎn)生時間短、表達量低,還易被蛋白酶降解,導致檢測信號波動大,難以標準化。從生物學特性而言,IL-6 是先天免疫反應的炎癥介質(zhì),可通過活化 JAK-STAT 和 NF-κB 通路驅動急性期反應,如誘導大腦產(chǎn)生前列腺素 E2(PGE2)觸發(fā)發(fā)熱,與熱原的致熱機制直接關聯(lián),是公認的發(fā)熱標志物。同時,MAT 法熱原檢測會輔以 IL-1β 和 TNF-α 監(jiān)測 ——IL-1β 反映單核細胞活化程度,TNF-α 提示炎癥放大效應,形成多因子協(xié)同體系。此外,IL-6 的 ELISA 試劑盒市場成熟度高、跨平臺兼容性強,而 IL-1β 和 TNF-α 的檢測方法在靈敏度和標準化上仍有局限,進一步奠定了 IL-6 的重要地位。
熱原有廣譜來源特征,革蘭陰性菌(內(nèi)毒素/LPS)致熱能力強,革蘭陽性菌、真菌、病毒均可產(chǎn)生。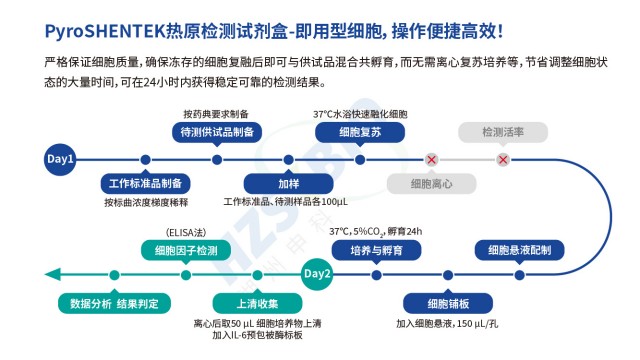
熱原檢測技術自 20 世紀初問世以來,經(jīng)歷了 “動物試驗→體外生化檢測→細胞生物學檢測” 的三次關鍵變革,每一次變革均推動檢測效率、準確性與全面性的提升。20 世紀初至中期,熱原檢測方法只有家兔熱原試驗,通過觀察家兔體溫變化篩查熱原,雖實現(xiàn)了廣譜檢測,但存在動物成本高、操作繁瑣、靈敏度低、種屬差異大等局限,難以滿足制藥行業(yè)快速發(fā)展需求。20 世紀 60 年代,鱟試驗法(LAL 法)的發(fā)明開啟了熱原檢測的 “體外生化時代”,利用鱟血變形細胞裂解物的凝血級聯(lián)反應檢測細菌內(nèi)毒素,靈敏度提升至 ng 級,檢測時間縮短至 1-2 小時,迅速成為制藥行業(yè)常規(guī)質(zhì)控方法;但該方法依賴鱟資源,易受 β- 葡聚糖干擾,且只能檢測內(nèi)毒素,無法覆蓋非內(nèi)毒素熱原。21 世紀以來,重組技術與細胞生物學技術的發(fā)展推動熱原檢測進入 “全熱原管控時代”:重組級聯(lián)試劑(rCR)與重組 C 因子試劑(rFC)通過基因工程技術制備,擺脫對鱟資源的依賴,消除葡聚糖干擾,實現(xiàn)標準化生產(chǎn);單核細胞活化反應測定(MAT)利用人源單核細胞檢測全類型熱原,填補非內(nèi)毒素熱原檢測空白,且結果更貼近人體實際反應。
熱原檢測MAT法可在96孔板中批量檢測,單批次實驗1.5天即可放行,家兔法需3-7天。江蘇高效熱原檢測技術升級鱟試驗法(LAL)法進行熱原檢測靈敏度高、操作方便,但只針對內(nèi)毒素,易受干擾且有 LER 現(xiàn)象。北京抗體藥物熱原檢測MAT法
PyroSHENTEK®熱原檢測試劑盒(MAT法)已完成 25 個品種樣品的檢測驗證,覆蓋單抗類、疫苗類、基因工程類、血液制品類、生化藥品類與注射液,結果顯示其適配性范圍廣但需關注部分樣品的干擾。疫苗類(如麻腮風聯(lián)合減毒活疫苗、人用狂犬病疫苗)、基因工程類(重組人促紅素、干擾素 α-2b)、血液制品類(人血白蛋白、凝血因子 Ⅷ)與注射液(生理鹽水、琥珀酰明膠)的加標回收率均在 50%-200% 范圍內(nèi),無明顯干擾,檢測結果可靠。單抗類(如貝伐珠單抗、阿達木單抗)、中藥注射液等樣品雖存在不同程度的抑制作用,需通過提高稀釋倍數(shù)(如稀釋至 MVD 上限)、超聲處理或添加中和劑消除抑制,優(yōu)化后回收率均可達標。此外,MAT 法可有效檢測非內(nèi)毒素熱原,如對貝伐珠單抗注射液中添加的酵母多糖(Zymosan,200μg/mL)、脂磷壁酸(LTA,10μg/mL),回收率分別達 113%、66.8%,證明其可解決傳統(tǒng)鱟試劑漏檢非內(nèi)毒素熱原的問題,尤其適用于高風險生物制品的熱原防控。
北京抗體藥物熱原檢測MAT法
相關新聞
- 上海高效熱原檢測MAT試劑盒 2025-12-19
- PG13宿主細胞蛋白(HCP)殘留檢測常見問題分析 2025-12-19
- CHO宿主細胞蛋白(HCP)殘留檢測方法學驗證 2025-12-19
- 北京高效內(nèi)毒素檢測商業(yè)化試劑盒 2025-12-19
- 北京通用型宿主細胞蛋白(HCP)殘留檢測抗體制備 2025-12-19
- 江蘇生物制品內(nèi)毒素檢測重組級聯(lián)試劑(rCR) 2025-12-19
- 北京通用型宿主細胞蛋白(HCP)殘留檢測 2025-12-19
- 浙江定制化宿主細胞蛋白(HCP)殘留檢測抗體覆蓋率驗證 2025-12-19
- SV40LTA&E1A宿主細胞殘留DNA檢測 2025-12-19
- 江蘇細菌內(nèi)毒素檢測結果判定 2025-12-19
推薦新聞
- 醫(yī)療器械結扎夾掛網(wǎng) 2025-12-20
- 山西國內(nèi)助膝器運動人群 2025-12-20
- 綜合醫(yī)院一體化臨床系統(tǒng)優(yōu)點 2025-12-20
- 洛龍口碑好的老年護理機構 2025-12-20
- 國內(nèi)固定式車輛通道監(jiān)測儀儀器維修 2025-12-20
- 濃縮銀杏的功效與作用 2025-12-20
- 浙江宮腔鏡醫(yī)學影像工作站安裝培訓 2025-12-20
- 云南核酸植絨拭子全國發(fā)貨 2025-12-20
- 福建智能聯(lián)網(wǎng)智能醫(yī)廢管理收集車直銷廠家 2025-12-20
- 什么是生物檢測試劑盒歡迎選購 2025-12-20