江西熱原檢測規范
來源:
發布時間:2025-11-17
PBMC(外周血單個核細胞)的復雜制備流程嚴重制約熱原檢測效率。首先,血源獲取受獻血者數量、時間及采集血液政策限制,無法按需即時獲取;其次,需嚴格執行 EP2.6.30 規定的標志物檢測,增加前期準備時間;再進行采集血液、分離單核細胞、凍存等環節需全程無菌操作,步驟繁瑣且易引入污染風險。相比之下,單核細胞系可工業化培養,制備流程簡單可控,能快速提供合格細胞,避免因 PBMC 制備延誤熱原檢測進度,更適配批量樣品的高效質控。單核細胞活化試驗(MAT)將熱原檢測從經驗性觀察,推進至受體-配體相互作用的分子本質。江西熱原檢測規范
生物制品(如單克隆抗體、重組蛋白、細胞因子)因基質成分復雜(含高濃度蛋白質、螯合劑、表面活性劑、緩沖鹽等),在熱原檢測過程中易出現“反應抑制”或“非特異性增強”現象,嚴重影響檢測結果準確性。選擇抗干擾能力更強的檢測方法至關重要,重組級聯試劑(rCR)因采用完整級聯反應路徑,抗干擾性優于天然 LAL;單核細胞活化反應測定(MAT)對復雜基質耐受性更高,通過適當稀釋即可消除多數干擾,因此生物制品熱原檢測常采用 “rCR 法(內毒素定量)+ MAT 法(全熱原篩查)” 的聯合方案,既保證內毒素檢測的準確性,又防控非內毒素熱原風險。
江西熱原檢測規范在藥品安全語境中,熱原特指細菌性熱原—微生物代謝產物、細菌尸體及內毒素的統稱。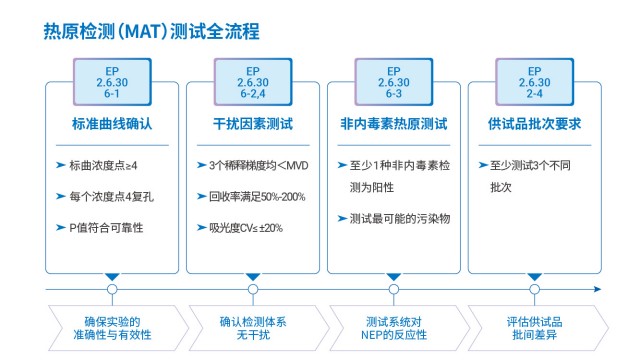
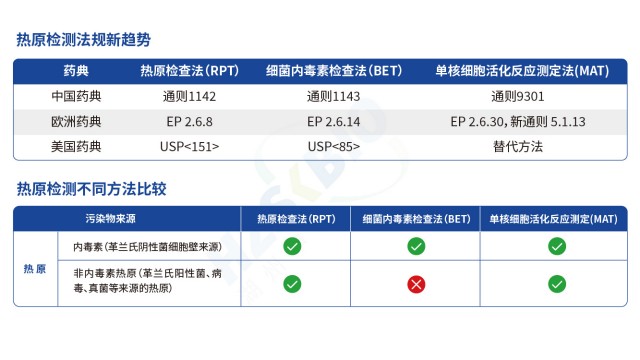
熱原是指微量即可引發恒溫動物體溫異常升高的物質,分為內源性(如細胞因子)與外源性兩類,外源性熱原又涵蓋微生物來源(革蘭氏陰性菌脂多糖 LPS、革蘭氏陽性菌脂磷壁酸 LTA、病毒、真菌等)與非微生物來源(灰塵、橡膠降解產物等)。傳統細菌內毒素檢查法(BET)只能檢測革蘭氏陰性菌的 LPS,無法覆蓋非內毒素熱原,而單核細胞活化試驗(MAT)可彌補這一缺陷。其原理是:熱原通過活化單核細胞表面的 Toll 樣受體(TLR,如 TLR4 識別 LPS、TLR2/TLR6 識別 LTA),啟動先天免疫反應,促使細胞釋放 IL-6、TNF-α 等促炎細胞因子;隨后采用 ELISA 法檢測 IL-6 濃度,結合 LPS 標準曲線推算樣品中總熱原含量,實現對內毒素與非內毒素熱原的同步檢測,契合《中國藥典》9301 指導原則中 全場景防控熱原風險”的要求。
傳統細菌內毒素檢查法(BET)只能檢測革蘭氏陰性菌的 LPS,無法識別革蘭氏陽性菌 LTA、真菌酵母多糖、病毒鞭毛蛋白等非內毒素熱原,存在漏檢風險;同時,部分樣品(如脂質體、表面活性劑制劑)會因內毒素吸附導致低內毒素回收(LER),BET法難以準確定量。MAT 法通過單核細胞表面的多種 TLR 受體(TLR1-TLR10),可識別不同類型熱原:TLR4 識別 LPS、TLR2/TLR6 識別 LTA 與酵母多糖、TLR5 識別鞭毛蛋白、TLR3 識別病毒 dsRNA 等,實現 “全熱原覆蓋”。湖州申科生物熱原檢測試劑盒(MAT法)的驗證數據顯示,其對不同濃度非內毒素熱原均有響應:如 0.1-100μg/mL 鞭毛蛋白可檢測到 0.005-0.035EU/mL熱原活性,0.1-10μg/mL LTA 對應 0.1-0.7EU/mL 熱原活性,1-100μg/mL 雷西莫特(TLR7/8 配體)對應 0.5-3.0EU/mL 熱原活性。此外,MAT法檢測的是熱原的生物活性(而非單純 LPS 含量),可避免 LER 導致的假陰性,為CGT等高風險產品提供更有保障的熱原檢測方案。
鱟試驗法(LAL)法進行熱原檢測靈敏度高、操作方便,但只針對內毒素,易受干擾且有 LER 現象。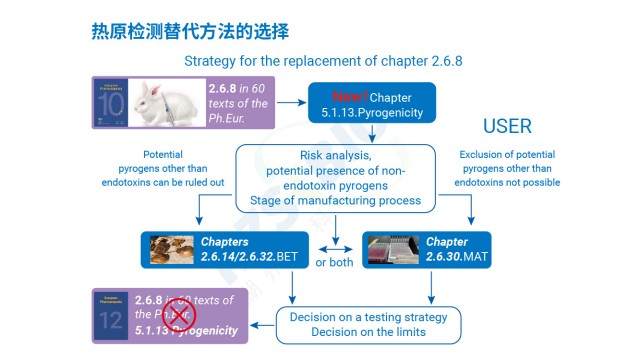
MAT法熱原檢測中,樣品與細胞共培養時長需嚴格控制,以保障炎癥因子分泌量穩定。說明書要求共培養 24 小時,雖未明確允差,但實驗驗證顯示,±30 分鐘的允差對結果無明顯影響 —— 細胞因子(如 IL-6)分泌具有時間依賴性,24 小時左右達到分泌平臺期,半小時差異不會導致分泌量大幅波動。若實驗室對結果穩定性要求極高(如 QC 放行檢測),建議嚴格按 24 小時操作,避免因時長差異引入誤差;若為預實驗(如樣品稀釋倍數摸索),±30 分鐘允差可接受,但需在記錄中注明實際培養時長。需注意的是,共培養時長不可超過 26 小時或短于 22 小時:過長會導致細胞活性下降(炎癥因子分泌減少),過短則未達分泌平臺期(檢測信號偏低),均可能導致熱原濃度低估。此外,培養環境需保持穩定(37℃、5% CO?),溫度波動會影響細胞代謝,間接導致共培養時長的實際效果偏離,因此需定期校準培養箱溫度,確保環境條件一致。
家兔法熱原試驗雖能篩查所有類別熱原,卻因周期長、成本高、靈敏度低而逐步被體外方法取代。醫療器械熱原檢測流程熱作為一種能引起人體溫異常升高的物質,一旦存在于藥品、醫療器械等產品中,將給患者帶來嚴重的健康風險。江西熱原檢測規范
MAT法(單核細胞活化反應測定)熱原檢測基于人體免疫反應機制設計,原理是:內毒素(革蘭氏陰性菌來源)與非內毒素熱原(革蘭氏陽性菌、霉菌、病毒等來源)進入人體后,會活化單核細胞或單核細胞系,使其釋放 IL-6、IL-1、IL-1β、TNF-α 等促炎細胞因子。檢測時將供試品與單核細胞 / 單核細胞系共孵育,再通過 ELISA 定量檢測釋放的 IL-6 含量,結合內毒素標準品繪制的標曲,即可判斷供試品中熱原含量是否符合規定,實現內毒素與非內毒素熱原的全覆蓋檢測。
江西熱原檢測規范
下一篇:
安徽生物制品支原體檢測NAT法
相關新聞
- 上海高效熱原檢測MAT試劑盒 2025-12-19
- 北京高效內毒素檢測商業化試劑盒 2025-12-19
- 北京通用型宿主細胞蛋白(HCP)殘留檢測抗體制備 2025-12-19
- 江蘇生物制品內毒素檢測重組級聯試劑(rCR) 2025-12-19
- 北京通用型宿主細胞蛋白(HCP)殘留檢測 2025-12-19
- 浙江定制化宿主細胞蛋白(HCP)殘留檢測抗體覆蓋率驗證 2025-12-19
- SV40LTA&E1A宿主細胞殘留DNA檢測 2025-12-19
- 江蘇細菌內毒素檢測結果判定 2025-12-19
- 上海通用型宿主細胞蛋白(HCP)殘留檢測方法學驗證 2025-12-19
- 北京ELISA法宿主細胞蛋白(HCP)殘留檢測抗體制備 2025-12-19
推薦新聞
- 佛山1470nm國產半導體激光治療儀廠家電話 2025-12-19
- 吳江區服務軟霧吸入器加盟連鎖店 2025-12-19
- 松江區定制吻合器工廠直銷 2025-12-19
- 深圳醫院智慧管理系統多少錢一套 2025-12-19
- 山西疫苗佐劑QS-21 2025-12-19
- 姑蘇區常見一次性注射器資費 2025-12-19
- 武漢本地活細胞成像分析系統直銷價格 2025-12-19
- 附近哪里有助腿器誠信合作 2025-12-19
- 銀杏葉片工廠 2025-12-19
- 珠海有實力的nmn定制廠家 2025-12-19