安徽生物制品支原體檢測國產(chǎn)替代
來源:
發(fā)布時間:2025-11-19
支原體 NAT 檢測中常見三類問題,其成因多與樣品基質(zhì)、操作規(guī)范或污染防控相關。1、樣品基質(zhì)干擾,高濃度 DMSO、人血白蛋白等凍存保護劑,高濃度細胞、DNA 碎片等復雜成分,會抑制檢測反應或干擾信號讀取。2、檢測曲線異常,表現(xiàn)為非特異性擴增圖譜,多因引物設計不當、反應條件優(yōu)化不足或試劑交叉污染導致。3、陰性污染,具體體現(xiàn)為無模板對照(NTC)、陰性對照(NCS)出現(xiàn)翹尾現(xiàn)象,主要源于實驗室分區(qū)不合理、操作流程不規(guī)范(如陰陽性樣本交叉處理)、耗材污染或環(huán)境氣溶膠污染,這些問題均會影響結果判定的準確性,需針對性解決。
歐洲藥典(EP)2.6.7 認可 NAT 法作為支原體檢測替代方法,需通過檢測限與可比性驗證。安徽生物制品支原體檢測國產(chǎn)替代
此前,支原體檢測依賴培養(yǎng)法和指示細胞培養(yǎng)法,這兩種傳統(tǒng)方法均被各國藥典列為基礎檢測手段,但存在明顯短板。培養(yǎng)法作為 “金標準”,需陽性活菌參照,每批次培養(yǎng)基需做靈敏度測試,完整合規(guī)檢測周期長達 21-35 天;指示細胞培養(yǎng)法同樣耗時 14-28 天,難以滿足新型生物制品快速上市、短貨架期的放行需求。更棘手的是,面對高蛋白等復雜樣品基質(zhì),傳統(tǒng)方法易受干擾或抑制,需額外增加傳代培養(yǎng)步驟,導致檢測時間再延長 2-3 周,嚴重影響生產(chǎn)效率,也難以適配新型生物制品的檢測場景。
江西疫苗產(chǎn)品支原體檢測驗證菌株支原體檢測試劑盒需覆蓋常見污染菌株,避免因菌株遺漏導致漏檢。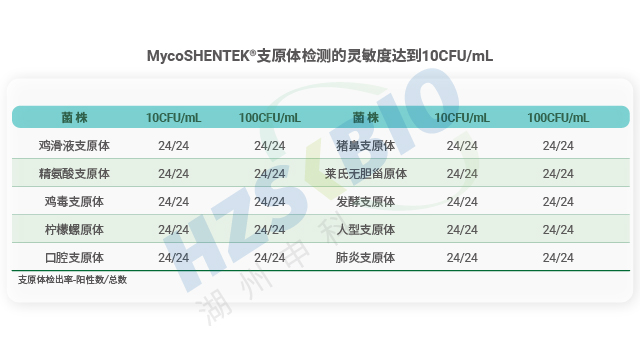
湖州申科構建了具有完備資質(zhì)的支原體技術服務平臺,為企業(yè)提供多元化支持。平臺擁有 BSL-2/P2 微生物實驗室備案資質(zhì),遵循 GMP-like 質(zhì)量體系,具備支原體培養(yǎng)法、指示細胞法與 qPCR 法的檢測及驗證能力,配備符合藥典要求的支原體標準菌株庫與高靈敏度培養(yǎng)基(含液體、固體、半流體)。企業(yè)已通過 ISO13485:2016 質(zhì)量管理體系認證(證書號 MD 709873),檢測中心獲得 CNAS 認證(注冊號 CNAS L21942),符合 ISO/IEC 17025:2017 標準,具備國際互認資質(zhì)。平臺可提供多元化技術服務,包括支原體 qPCR 法檢測能力建立、實驗員能力考核、質(zhì)量體系與流程搭建、實驗室設計方案優(yōu)化,以及樣品檢測(三種方法)、樣品適用性驗證、方法學驗證、傳統(tǒng)法與 qPCR 法比對、特殊菌株定制生產(chǎn)等,申報階段可配合客戶與監(jiān)管機構完成現(xiàn)場審計。
湖州申科的支原體驗證菌株以高穩(wěn)定性與合規(guī)性為重點優(yōu)勢,滿足 NAT 方法驗證需求。菌株來源可靠,均取自國內(nèi)外合規(guī)機構驗證菌株標準盤,溯源至美國 ATCC(口腔、肺炎支原體)、中國 CVCC(豬鼻支原體)等正規(guī)保藏機構,獲正式商用授權,標定濃度涵蓋 10CFU 與 100CFU。生產(chǎn)環(huán)境合規(guī),在 BSL-2 生物安全實驗室開展,符合國家生物安全法標準,針對不同菌株特性逐個優(yōu)化生產(chǎn)工藝,涵蓋超 10 種菌株的主代與工作代。質(zhì)控環(huán)節(jié)嚴謹,采用高靈敏度培養(yǎng)基(液體、固體、半流體),保障菌落易觀察分離與 CFU 計數(shù)準確性;凍存前后均通過固體平皿培養(yǎng)法測定 CFU,聯(lián)合合規(guī)機構建立數(shù)字 PCR 標定方法,經(jīng)實驗室間對比驗證,準確監(jiān)控 GC/CFU 比,確保菌株質(zhì)量達標。
疫苗病毒種子批支原體檢測需取全量樣品,建議進行 10mL 種子液提取,確保無漏檢。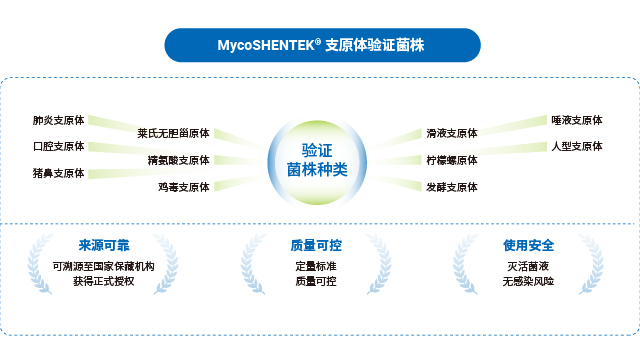
陰性翹尾是支原體 NAT 檢測中常見的異常現(xiàn)象,表現(xiàn)為 NCS 或 NTC 出現(xiàn)擴增信號,Ct 值多在 35~40 之間,需科學評估并處理。首先考慮污染因素,可能是陰性對照被陽性樣本、試劑或環(huán)境氣溶膠污染,建議立即復測,復測時使用帶濾芯低吸附 TIP 頭,嚴格執(zhí)行陰陽性分區(qū)操作,注重細節(jié)防控。其次需排除背景信號等非典型性擴增的干擾,避免誤判為污染。若前期驗證中頻繁出現(xiàn) NTC 或 NCS 擴增,且已徹底排除污染可能性,可結合已有實驗數(shù)據(jù)重新設置 Cut off 值,確保閾值線能有效區(qū)分真實陽性與背景信號,滿足實驗室檢測需求。
生物制品企業(yè)需建立支原體檢測質(zhì)量體系,滿足 GMP 與法規(guī)要求。上海免疫細胞產(chǎn)品支原體檢測指示細胞培養(yǎng)法湖州申科支原體檢測驗證菌株涵蓋 10 余種,滿足不同檢測場景驗證需求。安徽生物制品支原體檢測國產(chǎn)替代
為解決支原體檢測的污染難題,湖州申科推出AdvSHENTEK® 外源因子全自動核酸檢測分析系統(tǒng) + 一體化支原體檢測卡盒的組合方案,以全封閉設計從根源規(guī)避污染。該方案只需一步開蓋加樣,后續(xù)流程完全封閉運行,物理隔絕核酸氣溶膠污染,搭配 UNG 酶系統(tǒng)可進一步防止環(huán)境交叉污染,能節(jié)省 100% 污染排查時間。一體化檢測卡盒相當于單獨的迷你 qPCR 實驗室,集成試劑準備、樣品制備、擴增、分析全流程,無需復雜分區(qū)。同時,方案降低了對實驗環(huán)境和人員的要求,普通實驗室即可開展檢測,人員經(jīng)簡單培訓就能操作,徹底擺脫了傳統(tǒng) NAT 法對高技能人員和場地的依賴,大幅提升檢測結果的穩(wěn)定性。
安徽生物制品支原體檢測國產(chǎn)替代
上一篇
湖北疫苗熱原檢測
下一篇:
上海重組蛋白熱原檢測方法驗證
相關新聞
- 上海高效熱原檢測MAT試劑盒 2025-12-19
- PG13宿主細胞蛋白(HCP)殘留檢測常見問題分析 2025-12-19
- CHO宿主細胞蛋白(HCP)殘留檢測方法學驗證 2025-12-19
- 北京高效內(nèi)毒素檢測商業(yè)化試劑盒 2025-12-19
- 北京通用型宿主細胞蛋白(HCP)殘留檢測抗體制備 2025-12-19
- 江蘇生物制品內(nèi)毒素檢測重組級聯(lián)試劑(rCR) 2025-12-19
- 北京通用型宿主細胞蛋白(HCP)殘留檢測 2025-12-19
- 浙江定制化宿主細胞蛋白(HCP)殘留檢測抗體覆蓋率驗證 2025-12-19
- SV40LTA&E1A宿主細胞殘留DNA檢測 2025-12-19
- 江蘇細菌內(nèi)毒素檢測結果判定 2025-12-19
推薦新聞
- 洛龍口碑好的老年護理機構 2025-12-20
- 國內(nèi)固定式車輛通道監(jiān)測儀儀器維修 2025-12-20
- 濃縮銀杏的功效與作用 2025-12-20
- 福建智能聯(lián)網(wǎng)智能醫(yī)廢管理收集車直銷廠家 2025-12-20
- 什么是生物檢測試劑盒歡迎選購 2025-12-20
- 兒童青少年脊柱側(cè)彎支具24小時服務 2025-12-20
- 松江區(qū)國產(chǎn)生物檢測試劑盒 2025-12-20
- 山東效果助膝器怎么樣 2025-12-20
- 吉林包埋類型 2025-12-20
- 安徽無紡布加減孔膠帶廠家直供 2025-12-20