江蘇生物制品內(nèi)毒素檢測(cè)技術(shù)升級(jí)
來源:
發(fā)布時(shí)間:2025-09-30
2024年7月26日,《美國藥典》微生物委員會(huì)正式宣布,將第<86>章“使用重組試劑的細(xì)菌內(nèi)毒素測(cè)試”納入(USP-NF),該標(biāo)準(zhǔn)定于2025年5月正式生效。這一重要舉措不僅標(biāo)志著細(xì)菌內(nèi)毒素檢測(cè)領(lǐng)域從此正式邁入非動(dòng)物源試劑的嶄新發(fā)展階段,更契合了全球生命科學(xué)領(lǐng)域遵循的3R原則(即通過非動(dòng)物源技術(shù)替代動(dòng)物實(shí)驗(yàn)、減少實(shí)驗(yàn)動(dòng)物使用量、優(yōu)化實(shí)驗(yàn)流程以降低動(dòng)物痛苦)。此前傳統(tǒng)細(xì)菌內(nèi)毒素檢測(cè)多依賴從鱟血中提取的試劑,而鱟作為海洋瀕危“活化石”,其資源保護(hù)與檢測(cè)需求間的矛盾長期存在;如今重組級(jí)聯(lián)試劑(rCR)憑借技術(shù)創(chuàng)新成功替代傳統(tǒng)鱟血,在有效守護(hù)藍(lán)血鱟的生態(tài)未來、緩解資源依賴?yán)Ь车耐瑫r(shí),也為藥品生產(chǎn)中的內(nèi)毒素質(zhì)量控制和用藥安全保障,提供了更先進(jìn)、更穩(wěn)定且具備長期可持續(xù)性的解決方案。
內(nèi)毒素檢測(cè)凝膠法實(shí)驗(yàn)需西林瓶等耗材,確保無外源內(nèi)毒素污染檢測(cè)。江蘇生物制品內(nèi)毒素檢測(cè)技術(shù)升級(jí)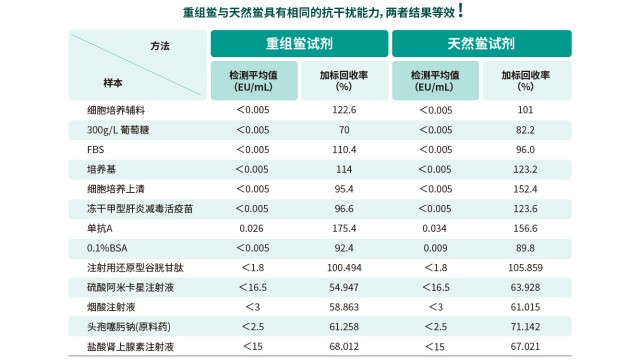
湖州申科生物重組級(jí)聯(lián)試劑(rCR)采用基因工程技術(shù)合成,完全模擬了天然鱟試劑中的酶促級(jí)聯(lián)放大反應(yīng)。重組鱟試劑反應(yīng)體系中包含重組C因子、重組B因子和重組凝固酶原。當(dāng)供試品中存在內(nèi)毒素,重組C因子識(shí)別內(nèi)毒素后活化,會(huì)依次級(jí)聯(lián)活化下游重組B因子和重組凝固酶原。凝固酶原轉(zhuǎn)化為具有生物活性的凝固酶后,識(shí)別并催化下游帶顯色基團(tuán)的底物產(chǎn)生顯色反應(yīng)。顯色反應(yīng)的強(qiáng)度和內(nèi)毒素濃度成正相關(guān),從而定量檢測(cè)內(nèi)毒素。本產(chǎn)品用于定量測(cè)定人用和動(dòng)物用注射藥物、生物制品及醫(yī)療器械等樣品中的細(xì)菌內(nèi)毒素的含量。
江蘇非動(dòng)物源內(nèi)毒素檢測(cè)LER現(xiàn)象在醫(yī)藥、生物制品及醫(yī)療器械等諸多領(lǐng)域,細(xì)菌內(nèi)毒素檢測(cè)是保障產(chǎn)品質(zhì)量與安全的關(guān)鍵環(huán)節(jié)。
重組級(jí)聯(lián)試劑作為內(nèi)毒素檢測(cè)鱟試劑的理想替代方案,其具備的優(yōu)勢(shì)有:①優(yōu)化的G因子級(jí)聯(lián)反應(yīng),無G因子旁路干擾。采用基因重組技術(shù)表達(dá)鱟血細(xì)胞中的C因子(Factor C)、B因子(Factor B)和凝固酶原(Proclotting enzyme),無G因子旁路干擾,排除1,3-β-D葡聚糖假陽性風(fēng)險(xiǎn)。②依然采用動(dòng)態(tài)顯色法原理,可沿用天然鱟試劑檢測(cè)設(shè)備。重組級(jí)聯(lián)試劑(rCR),與天然鱟(動(dòng)態(tài)顯色法)具有相同的操作流程、檢測(cè)設(shè)備、分析方法,用戶可以沿用天然鱟的儀器、軟件、耗材、人員培訓(xùn)、驗(yàn)收程序等,無需投入額外成本。③具有與天然鱟的相同反應(yīng)機(jī)制,檢測(cè)結(jié)果具有等效性。完全模擬了天然鱟試劑的酶聯(lián)反應(yīng),由3種蛋白組成的級(jí)聯(lián)反應(yīng)機(jī)制提供了信號(hào)放大的過程,確保了檢測(cè)的準(zhǔn)確性和靈敏度。湖州申科按照藥典要求進(jìn)行替代方法驗(yàn)證,無縫銜接技術(shù)轉(zhuǎn)移,助力用戶從方法驗(yàn)證到工藝落地,從數(shù)據(jù)合規(guī)到全球申報(bào)。
實(shí)驗(yàn)數(shù)據(jù)充分證明,內(nèi)毒素檢測(cè)重組級(jí)聯(lián)試劑(rCR)與天然鱟試劑的檢測(cè)結(jié)果具有高度等效性,可實(shí)現(xiàn)方法無縫切換。對(duì)細(xì)胞培養(yǎng)輔料、凍干甲型肝炎疫苗、單抗 A/B 等 8 類代表性樣品的平行檢測(cè)顯示,rCR 的檢測(cè)平均值為 0.001-0.026EU/mL,天然鱟試劑為 0.002-0.034EU/mL,兩者偏差≤0.003EU/mL。加標(biāo)回收率方面,rCR 為 70%-175.4%,天然鱟試劑為 82.2%-156.6%,均處于 50%-200% 的合格范圍。批內(nèi)精密度上,rCR 的 CV 值為 0.524%-14.716%,天然鱟試劑為 0.908%-12.348%,均滿足法規(guī)對(duì)精密度的要求。這種等效性確保了實(shí)驗(yàn)室在切換至重組試劑時(shí),歷史數(shù)據(jù)和工藝控制標(biāo)準(zhǔn)的連續(xù)性,降低方法轉(zhuǎn)換風(fēng)險(xiǎn)。
重組級(jí)聯(lián)試劑(rCR)抗干擾能力強(qiáng)于重組 C 因子(rFC),適配高蛋白、疫苗等復(fù)雜樣本檢測(cè)。
內(nèi)毒素檢測(cè)的實(shí)驗(yàn)方案需遵循“標(biāo)曲可靠性驗(yàn)證(靈敏度復(fù)核)-稀釋倍數(shù)計(jì)算-干擾試驗(yàn)”的完整流程,以保障檢測(cè)結(jié)果準(zhǔn)確合規(guī)。首先進(jìn)行標(biāo)曲可靠性試驗(yàn),用標(biāo)準(zhǔn)內(nèi)毒素制備至少3個(gè)濃度的稀釋液(相鄰濃度間稀釋倍數(shù)不超過10,下限濃度不低于鱟試劑標(biāo)示檢測(cè)限),每濃度設(shè) 3 支平行管,同時(shí)做2支陰性對(duì)照;當(dāng)陰性對(duì)照的吸光度小于或透光率大于標(biāo)準(zhǔn)曲線下限的檢測(cè)值或反應(yīng)時(shí)間大于標(biāo)準(zhǔn)曲線下限的反應(yīng)時(shí)間,對(duì)數(shù)據(jù)進(jìn)行線性回歸,相關(guān)系數(shù)r的幅值≥0.980時(shí)試驗(yàn)方有效,否則需重新操作。接著按公式 L=K/M 確定樣本內(nèi)毒素限值,K 值依給藥途徑而定,M結(jié)合人均60kg體重、1.62m2 體表面積及上限給藥劑量計(jì)算,也可參考藥典行標(biāo)。隨后明確有效稀釋上限倍數(shù)(MVD),即供試品允許稀釋的上限倍數(shù),確保在此范圍內(nèi)檢測(cè)限值。再開展樣本干擾試驗(yàn),制備供試品溶液(A)、供試品加標(biāo)溶液(B,加標(biāo)濃度為標(biāo)曲中點(diǎn))、標(biāo)準(zhǔn)曲線溶液(C)及陰性對(duì)照(D),按公式 R=(Cs-Ct)/λm×100%計(jì)算加標(biāo)回收率,50%-200%為合格;若鱟試劑、生產(chǎn)工藝等發(fā)生變化,需重新進(jìn)行干擾試驗(yàn),保障內(nèi)毒素檢測(cè)的可靠性。
進(jìn)行重組級(jí)聯(lián)試劑時(shí),不同酶標(biāo)儀檢測(cè)樣本 Onset time 有差異,因信號(hào)采集方式和靈敏度不同。廣東生物制品內(nèi)毒素檢測(cè)鱟試劑塑料器皿對(duì)內(nèi)毒素吸附力強(qiáng),制備內(nèi)毒素工作標(biāo)準(zhǔn)品(CSE)稀釋液建議用硼硅酸鹽玻璃管。江蘇生物制品內(nèi)毒素檢測(cè)技術(shù)升級(jí)
如何準(zhǔn)備樣品進(jìn)行內(nèi)毒素檢測(cè)呢?測(cè)試前,需要根據(jù)樣品實(shí)際情況進(jìn)行樣本前處理。大多數(shù)樣品只需要稀釋,使用內(nèi)毒素檢測(cè)試劑盒進(jìn)行測(cè)試即可。如果樣品有蛋白酶干擾并導(dǎo)致假陽性結(jié)果,建議對(duì)樣品稀釋并70°C加熱5-15分鐘進(jìn)行熱滅活處理。如需要,可以對(duì)滅活樣品進(jìn)行進(jìn)一步稀釋后檢測(cè)。如果樣品可能含有受β-葡聚糖,建議使用抗增液。β-葡聚糖可能來自酵母和纖維素材料。如果樣品中因含有內(nèi)毒素結(jié)合物而存在抑制,可以嘗試使用分散劑。
江蘇生物制品內(nèi)毒素檢測(cè)技術(shù)升級(jí)
相關(guān)新聞
- 上海高效熱原檢測(cè)MAT試劑盒 2025-12-19
- PG13宿主細(xì)胞蛋白(HCP)殘留檢測(cè)常見問題分析 2025-12-19
- CHO宿主細(xì)胞蛋白(HCP)殘留檢測(cè)方法學(xué)驗(yàn)證 2025-12-19
- 北京高效內(nèi)毒素檢測(cè)商業(yè)化試劑盒 2025-12-19
- 北京通用型宿主細(xì)胞蛋白(HCP)殘留檢測(cè)抗體制備 2025-12-19
- 江蘇生物制品內(nèi)毒素檢測(cè)重組級(jí)聯(lián)試劑(rCR) 2025-12-19
- 北京通用型宿主細(xì)胞蛋白(HCP)殘留檢測(cè) 2025-12-19
- 浙江定制化宿主細(xì)胞蛋白(HCP)殘留檢測(cè)抗體覆蓋率驗(yàn)證 2025-12-19
- SV40LTA&E1A宿主細(xì)胞殘留DNA檢測(cè) 2025-12-19
- 江蘇細(xì)菌內(nèi)毒素檢測(cè)結(jié)果判定 2025-12-19
推薦新聞
- 四川影像的采集錄制醫(yī)學(xué)影像工作站24小時(shí)服務(wù) 2025-12-20
- 天津高性價(jià)比QS-21現(xiàn)貨供應(yīng) 2025-12-20
- 新疆Fab合成文庫公司推薦 2025-12-20
- 河南CRET技術(shù)CD因子檢測(cè) 2025-12-20
- 南京進(jìn)口的全自動(dòng)核酸提取儀批發(fā)廠家 2025-12-20
- PCM170表面污染測(cè)量儀 2025-12-20
- 廣西電池模組制造 2025-12-20
- 南通國內(nèi)智能醫(yī)療穿戴設(shè)備規(guī)劃 2025-12-20
- 作用六字真言香囊地方 2025-12-20
- 上海定制式助聽器多少錢 2025-12-20