-
 廣東非動物源內毒素檢測凝膠法鱟試劑
廣東非動物源內毒素檢測凝膠法鱟試劑內毒素檢測常與熱原檢測混淆,二者既有關聯又有區別:熱原是指所有能引起發熱的物質(包括內毒素、病毒、真菌等),通過傳統家兔熱原試驗檢測;內毒素是熱原的主要成分(占 90% 以上),檢測更具特異性。目前,家兔熱原試驗因操作復雜、動物成本高,已逐漸被單核細胞活化反應測定法(MAT)替代,但部分產品(如放射性質藥物、血液制品)仍需保留家兔試驗作為補充。法規要求內毒素檢測結果需與熱原風險關聯,若內毒素檢測合格但臨床出現熱原反應,需排查是否存在非內毒素類熱原,通過聯合檢測確保產品安全性。 外源性熱原含細菌內毒素、脂磷壁酸、酵母多糖等,單核細胞活化反應檢查法可檢出全部熱原。廣東非動物源內毒素檢測凝膠法鱟...
2025-10-01 -
 廣東合規性內毒素檢測低內毒素回收
廣東合規性內毒素檢測低內毒素回收重組級聯試劑作為內毒素檢測鱟試劑的理想替代方案,其具備的優勢有:①優化的G因子級聯反應,無G因子旁路干擾。采用基因重組技術表達鱟血細胞中的C因子(Factor C)、B因子(Factor B)和凝固酶原(Proclotting enzyme),無G因子旁路干擾,排除1,3-β-D葡聚糖假陽性風險。②依然采用動態顯色法原理,可沿用天然鱟試劑檢測設備。重組級聯試劑(rCR),與天然鱟(動態顯色法)具有相同的操作流程、檢測設備、分析方法,用戶可以沿用天然鱟的儀器、軟件、耗材、人員培訓、驗收程序等,無需投入額外成本。③具有與天然鱟的相同反應機制,檢測結果具有等效性。完全模擬了天然鱟試劑的酶聯反應,...
2025-10-01 -
 內毒素檢測重組級聯試劑(rCR)
內毒素檢測重組級聯試劑(rCR)低內毒素回收(LER)又稱內毒素掩蔽,是指無菌制劑(尤其蛋白類生物制劑)進行內毒素檢測時,加標內毒素的回收率<50% 的現象,且無法通過稀釋排除,區別于傳統檢測干擾。LER 會導致內毒素污染被低估,已被全球監管機構重點關注:FDA 2013 年要求生物藥 BLA 申報時提交 LER 研究報告;EMA 2023 年明確含表面活性劑(如吐溫)或螯合劑(如 EDTA)的制劑需提供 LER 數據;中國藥典 2025 版 9251 通則也新增 LER 內容,與國際接軌。這些要求促使企業優化內毒素檢測流程,避免因 LER 導致的檢測偏差,確保藥品安全。 細菌內毒素是革蘭氏陰性菌細胞壁脂多糖,細菌死亡裂...
2025-09-30 -
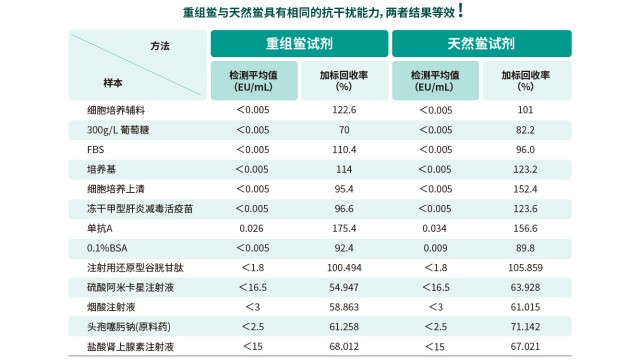 江蘇非動物源內毒素檢測動態顯色法鱟試劑
江蘇非動物源內毒素檢測動態顯色法鱟試劑當實驗室更換內毒素檢測方法或更換試劑供應商時,需進行方法比對與橋接驗證。比對實驗需選取至少 3批代表性樣品,分別用新舊方法檢測,計算結果相關性(如相關系數 R2≥0.95)和偏差(≤20%)。橋接驗證還需評估新方法的特異性、靈敏度是否與舊方法一致,如確認對高風險樣品(如含 β- 葡聚糖的樣品)的抗干擾能力相當。若方法變更涉及法規申報產品,需將驗證數據納入申報資料,證明變更后方法仍能有效控制內毒素風險,符合 FDA、NMPA 等監管機構對方法變更的合規性要求。 細菌內毒素是革蘭氏陰性菌細胞壁脂多糖,細菌死亡裂解釋放,微量級即致人體發熱、休克等威脅。江蘇非動物源內毒素檢測動態顯色法鱟試劑 湖...
2025-09-30 -
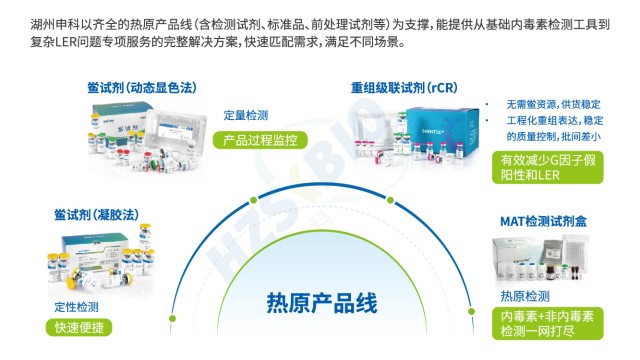 上海高效內毒素檢測風險評估
上海高效內毒素檢測風險評估內毒素檢測中,樣品中的蛋白質或酶的修飾作用易破壞鱟試劑的反應體系,導致檢測結果失真。鱟試劑檢測內毒素的本質是一系列絲氨酸蛋白酶的酶促放大過程,若樣品中存在氧化劑、抗氧化劑、蛋白水解劑或專一失活劑,會直接滅活反應所需的酶;而乙醇、苯酚等物質則會導致蛋白質變性,同樣抑制反應進程。例如,某些生物制品中含有的蛋白水解酶,可能提前降解鱟試劑中的蛋白酶,使內毒素無法被正常檢測。為消除這類干擾,需優先限制樣品中抑制物的含量:可采用內毒素檢查用水稀釋樣品,降低抑制物濃度;對耐熱的抑制物(如部分蛋白水解酶),可通過加熱滅活處理(如 56℃孵育 30 分鐘)破壞其活性;若樣品基質復雜,還可使用超濾技術分離內毒...
2025-09-30 -
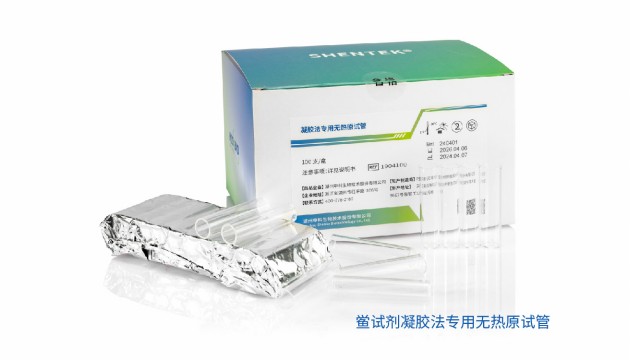 廣東血液制品內毒素檢測操作步驟
廣東血液制品內毒素檢測操作步驟醫療器械(如輸液器、注射器、植入式設備)若攜帶內毒素,可能通過血液、組織接觸引發異常反應或炎癥反應。其檢測需遵循 “模擬臨床使用” 原則:采用浸提液(如 0.9% 氯化鈉溶液或注射用水)在 37℃±1℃下浸提器械表面內毒素,再通過 LAL 或 rFC 法檢測浸提液。不同器械的內毒素限值差異明顯:一次性輸液器需≤0.5 EU/device,植入式心臟瓣膜則要求更嚴格(≤0.06 EU/device)。檢測時需注意器械材質對浸提效率的影響,如塑料類器械可能吸附內毒素,需優化浸提時間(通常≥1 小時)或采用超聲輔助提取,確保殘留內毒素被充分檢出。 在醫藥、生物制品及醫療器械等諸多領域,細菌內毒素...
2025-09-30 -
 北京醫療器械內毒素檢測操作步驟
北京醫療器械內毒素檢測操作步驟重組級聯試劑(rCR)通過完整模擬天然鱟試劑的酶促級聯反應路徑,實現高效且特異的內毒素檢測。其反應機制為:內毒素首先活化重組 C 因子,活化的 C 因子進一步活化重組 B 因子,隨后活化重組凝固酶原轉化為凝固酶,再催化顯色底物產生黃色信號(405nm 波長可檢測)。這一級聯放大過程有效提升了檢測靈敏度,即使微量內毒素也能產生可識別信號。與單因子的重組 C 因子法(rFC)相比,rCR 的多因子級聯反應抗干擾能力更強,尤其對復雜基質樣品(如高蛋白單抗、疫苗)表現更優。同時,rCR 剔除了天然鱟試劑中的 G 因子,避免了與 β-D 葡聚糖的非特異性反應,從根本上減少假陽性結果,保障檢測數據的可...
2025-09-30 -
 浙江血液制品內毒素檢測低內毒素回收
浙江血液制品內毒素檢測低內毒素回收湖州申科建立了標準化的低內毒素回收(LER)技術服務流程,全周期支撐內毒素檢測優化:7 個自然日內完成客戶溝通與 LER 確認,用天然鱟、重組鱟等方法檢測并出具報告;60 個自然日開展方法開發,分析 LER 成因(如螯合劑、蛋白質 IP)并研究去掩蔽方案;30 個自然日進行 HTS 驗證,完成 3 批 LER 實驗與干擾實驗,交付穩定試劑盒、操作規程及培訓;再協助方法轉移與 cGMP 驗證。流程每環節均圍繞內毒素檢測展開,確保企業高效解決 LER 問題,滿足法規要求。 重組鱟試劑無動物源,支持 3R 原則,批次差異小,適配動態顯色法酶標儀。浙江血液制品內毒素檢測低內毒素回收 血液制品(如...
2025-09-30 -
 浙江重組蛋白內毒素檢測技術升級
浙江重組蛋白內毒素檢測技術升級內毒素檢測結果誤差可能源于多環節:試劑方面,鱟試劑(LAL )或試劑批間差異、過期試劑活性下降會導致結果偏差,需通過試劑驗收(如陽性對照回收率驗證)確保質量;操作方面,實驗器具未除熱原(如玻璃器皿未干熱滅菌)、加樣體積不準確會引入污染或誤差,需嚴格執行 SOP(如器皿 250℃干熱滅菌≥30 分鐘);環境方面,實驗室空氣中的微生物孢子、粉塵可能污染樣品,需在潔凈工作臺操作并設置陰性對照。此外,反應溫度波動(偏離 37℃±1℃)會影響酶活性,需使用恒溫孵育器精確控溫,確保反應條件穩定。 細菌內毒素檢測中,rCR 加標回收率穩定在 50%-200% 藥典范圍,可準確完成檢測。浙江重組蛋白內毒素...
2025-09-30 -
 江蘇生物制品內毒素檢測技術升級
江蘇生物制品內毒素檢測技術升級2024年7月26日,《美國藥典》微生物委員會正式宣布,將第<86>章“使用重組試劑的細菌內毒素測試”納入(USP-NF),該標準定于2025年5月正式生效。這一重要舉措不僅標志著細菌內毒素檢測領域從此正式邁入非動物源試劑的嶄新發展階段,更契合了全球生命科學領域遵循的3R原則(即通過非動物源技術替代動物實驗、減少實驗動物使用量、優化實驗流程以降低動物痛苦)。此前傳統細菌內毒素檢測多依賴從鱟血中提取的試劑,而鱟作為海洋瀕危“活化石”,其資源保護與檢測需求間的矛盾長期存在;如今重組級聯試劑(rCR)憑借技術創新成功替代傳統鱟血,在有效守護藍血鱟的生態未來、緩解資源依賴困境的同時,也為藥品生產中...
2025-09-30 -
 廣東抗體藥物內毒素檢測技術服務
廣東抗體藥物內毒素檢測技術服務在開展內毒素檢測時,樣品的 pH 值與二價離子(Mg2?、Ca2?)水平是影響鱟試劑酶促反應的關鍵因素,直接關系檢測結果的準確性。鱟試劑檢測內毒素依賴絲氨酸蛋白酶的級聯放大反應,該反應的合適 pH 值范圍為 6.0-8.0,若樣品過酸或過堿,會快速降低酶活性,甚至導致酶徹底失活,進而出現內毒素檢測假陰性。針對這一問題,可使用 0.1N 或更低濃度的 HCl/NaOH 溶液,將樣品 pH 值準確調節至適宜區間,為反應提供穩定環境。同時,二價離子是反應必需的輔助因子:Mg2?是內毒素活化鱟試劑的關鍵,缺乏會直接阻斷反應啟動;Ca2?雖參與酶促反應,但濃度過高會反向抑制反應效率。若樣品中含有肝素...
2025-09-30 -
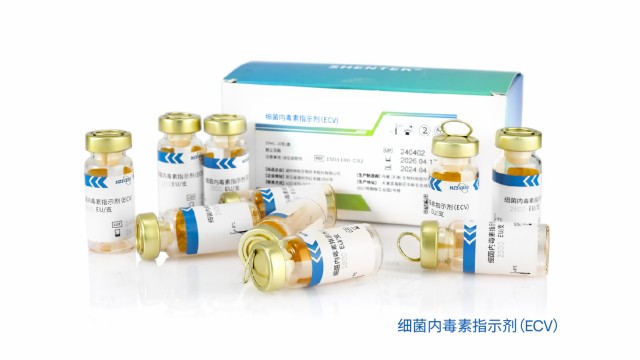 江蘇合規性內毒素檢測技術服務
江蘇合規性內毒素檢測技術服務湖州申科生物重組級聯試劑(rCR)采用基因工程技術合成,完全模擬了天然鱟試劑中的酶促級聯放大反應。重組鱟試劑反應體系中包含重組C因子、重組B因子和重組凝固酶原。當供試品中存在內毒素,重組C因子識別內毒素后活化,會依次級聯活化下游重組B因子和重組凝固酶原。凝固酶原轉化為具有生物活性的凝固酶后,識別并催化下游帶顯色基團的底物產生顯色反應。顯色反應的強度和內毒素濃度成正相關,從而定量檢測內毒素。本產品用于定量測定人用和動物用注射藥物、生物制品及醫療器械等樣品中的細菌內毒素的含量。 內毒素檢測需關注制劑成分,螯合劑和表面活性劑可能誘發“低內毒素回收(LER)”。江蘇合規性內毒素檢測技術服務 20...
2025-09-30 -
 原料藥內毒素檢測低內毒素回收
原料藥內毒素檢測低內毒素回收湖州申科生物細菌內毒素工作標準品(CSE)源自大腸桿菌(E.coli O111:B4),經過提取精制獲得脂多糖,并以細菌內毒素國家標準品為基準標定效價,每支效價處于 10 - 100EU ,量值準確且可靠。在工業內毒素檢測中,該標準品應用廣且關鍵。首先,能用于鱟試劑靈敏度復核實驗,幫助檢測人員準確確認鱟試劑對細菌內毒素的敏感程度,保障檢測方法的有效性;其次,可開展干擾試驗,評估樣品中可能存在的干擾物質對檢測結果的影響,以便優化檢測流程和方法;再者,能充當各種陽性對照,為檢測過程提供參照,確保檢測結果的準確性與可靠性。這款標準品不僅適用于凝膠法鱟試劑系列實驗,在光度法鱟試劑系列實驗中同樣能發...
2025-09-30 -
 北京醫療器械內毒素檢測鱟試劑
北京醫療器械內毒素檢測鱟試劑湖州申科建立了標準化的低內毒素回收(LER)技術服務流程,全周期支撐內毒素檢測優化:7 個自然日內完成客戶溝通與 LER 確認,用天然鱟、重組鱟等方法檢測并出具報告;60 個自然日開展方法開發,分析 LER 成因(如螯合劑、蛋白質 IP)并研究去掩蔽方案;30 個自然日進行 HTS 驗證,完成 3 批 LER 實驗與干擾實驗,交付穩定試劑盒、操作規程及培訓;再協助方法轉移與 cGMP 驗證。流程每環節均圍繞內毒素檢測展開,確保企業高效解決 LER 問題,滿足法規要求。 重組級聯試劑(rCR)適用于細胞培養輔料、單抗、凍干疫苗等樣本,內毒素檢測適用范圍廣。北京醫療器械內毒素檢測鱟試劑 血液...
2025-09-29 -
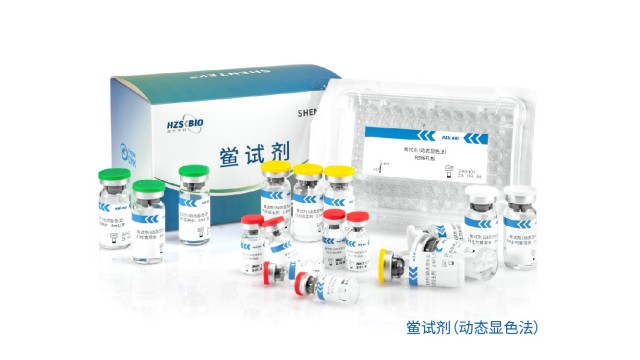 江蘇原料藥內毒素檢測風險評估
江蘇原料藥內毒素檢測風險評估如何準備樣品進行內毒素檢測呢?測試前,需要根據樣品實際情況進行樣本前處理。大多數樣品只需要稀釋,使用內毒素檢測試劑盒進行測試即可。如果樣品有蛋白酶干擾并導致假陽性結果,建議對樣品稀釋并70°C加熱5-15分鐘進行熱滅活處理。如需要,可以對滅活樣品進行進一步稀釋后檢測。如果樣品可能含有受β-葡聚糖,建議使用抗增液。β-葡聚糖可能來自酵母和纖維素材料。如果樣品中因含有內毒素結合物而存在抑制,可以嘗試使用分散劑。 內毒素檢測需關注制劑成分,螯合劑和表面活性劑可能誘發“低內毒素回收(LER)”。江蘇原料藥內毒素檢測風險評估 重組級聯試劑作為內毒素檢測鱟試劑的理想替代方案,其具備的優勢有:①優化的...
2025-09-29 -
 浙江重組蛋白內毒素檢測風險評估
浙江重組蛋白內毒素檢測風險評估針對單核細胞活化反應測定法(MAT)通過檢測內毒素的生物活性,有效規避低內毒素回收(LER)對內毒素檢測的影響。其原理是:熱原(包括被掩蔽的 LPS)活化單核細胞表面的 TLR 受體,釋放 IL-6 等細胞因子,通過 ELISA 檢測 IL-6 濃度,結合標準曲線推算熱原含量。即使 LPS 因 LER 改變超分子結構,只要仍具生物活性,就能被 MAT 法識別。這種 “檢測活性而非結構” 的特性,使 MAT 法成為 LER 場景下內毒素檢測的重要補充,與其他方法協同構建高效可靠的熱原防控體系。 在醫藥、生物制品及醫療器械等諸多領域,細菌內毒素檢測是保障產品質量與安全的關鍵環節。浙江重組蛋白內...
2025-09-29 -
 北京生物制品內毒素檢測合規申報
北京生物制品內毒素檢測合規申報內毒素檢測重組級聯試劑(rCR)與天然鱟試劑在原料、性能和可持續性上存在本質區別。原料方面,天然鱟試劑依賴鱟血采集,受動物資源限制,而 rCR 通過基因工程表達 C、B 因子及凝固酶原,無動物源性,供應穩定。特異性上,天然鱟試劑因含 G 因子,易與 β-D 葡聚糖反應產生假陽性,而 rCR 剔除 G 因子,只對內毒素特異性響應,從機制上消除干擾。批間一致性方面,天然鱟試劑受鱟個體差異影響,批間 CV 值較高;rCR 成分明確且生產工藝標準化,批間差異明顯降低,CV 值≤15%。兩者靈敏度相當(0.005EU/mL),但 rCR 無需面臨鱟資源政策限制,更符合動物福利趨勢和長期質控需求,是天...
2025-09-29 -
 北京細菌內毒素檢測結果判定
北京細菌內毒素檢測結果判定針對單核細胞活化反應測定法(MAT)通過檢測內毒素的生物活性,有效規避低內毒素回收(LER)對內毒素檢測的影響。其原理是:熱原(包括被掩蔽的 LPS)活化單核細胞表面的 TLR 受體,釋放 IL-6 等細胞因子,通過 ELISA 檢測 IL-6 濃度,結合標準曲線推算熱原含量。即使 LPS 因 LER 改變超分子結構,只要仍具生物活性,就能被 MAT 法識別。這種 “檢測活性而非結構” 的特性,使 MAT 法成為 LER 場景下內毒素檢測的重要補充,與其他方法協同構建高效可靠的熱原防控體系。 進行重組級聯試劑時,不同酶標儀檢測樣本 Onset time 有差異,因信號采集方式和靈敏度不同。...
2025-09-29 -
 血液制品內毒素檢測重組級聯試劑(rCR)
血液制品內毒素檢測重組級聯試劑(rCR)內毒素檢測常與熱原檢測混淆,二者既有關聯又有區別:熱原是指所有能引起發熱的物質(包括內毒素、病毒、真菌等),通過傳統家兔熱原試驗檢測;內毒素是熱原的主要成分(占 90% 以上),檢測更具特異性。目前,家兔熱原試驗因操作復雜、動物成本高,已逐漸被單核細胞活化反應測定法(MAT)替代,但部分產品(如放射性質藥物、血液制品)仍需保留家兔試驗作為補充。法規要求內毒素檢測結果需與熱原風險關聯,若內毒素檢測合格但臨床出現熱原反應,需排查是否存在非內毒素類熱原,通過聯合檢測確保產品安全性。 β- 葡聚糖刺激 G 因子致假陽性,用含抗增液的鱟試劑可優化內毒素檢測結果。血液制品內毒素檢測重組級聯試劑(rCR...
2025-09-29 -
 北京生物制品內毒素檢測法規要求
北京生物制品內毒素檢測法規要求低內毒素回收(LER)與傳統鱟試劑干擾(抑制 / 增強)在多維度存在差異,準確區分對優化內毒素檢測至關重要。表現上,LER 是內毒素回收率<50%,傳統干擾是反應抑制或增強;成因上,LER 由螯合劑 + 表面活性劑協同或蛋白質電荷結合引發,傳統干擾因 pH、β- 葡聚糖等導致;排除方式上,LER 時間依賴且無法稀釋解決,傳統干擾濃度依賴且可通過稀釋緩解;確認方法上,LER 需通過保存時間研究(HTS),傳統干擾按藥典干擾實驗評估。明確這些區別能幫助企業排查內毒素檢測異常,避免誤將 LER 當作普通干擾處理。 開展細菌內毒素檢測的操作過程,需防止樣品受到外源性污染。北京生物制品內毒素檢測法規...
2025-09-29 -
 北京血液制品內毒素檢測低內毒素回收
北京血液制品內毒素檢測低內毒素回收內毒素檢測常與熱原檢測混淆,二者既有關聯又有區別:熱原是指所有能引起發熱的物質(包括內毒素、病毒、真菌等),通過傳統家兔熱原試驗檢測;內毒素是熱原的主要成分(占 90% 以上),檢測更具特異性。目前,家兔熱原試驗因操作復雜、動物成本高,已逐漸被單核細胞活化反應測定法(MAT)替代,但部分產品(如放射性質藥物、血液制品)仍需保留家兔試驗作為補充。法規要求內毒素檢測結果需與熱原風險關聯,若內毒素檢測合格但臨床出現熱原反應,需排查是否存在非內毒素類熱原,通過聯合檢測確保產品安全性。 內毒素檢查用水經二次精制,無菌無熱原,避免檢測假陽假陰。北京血液制品內毒素檢測低內毒素回收 湖州申科建立了標準化...
2025-09-29 -
 江蘇醫療器械內毒素檢測常見問題分析
江蘇醫療器械內毒素檢測常見問題分析低內毒素回收(LER)的主要形成機制之一是螯合劑與非離子表面活性劑的協同作用,直接影響內毒素檢測結果。第一步,樣品中的螯合劑(如檸檬酸鹽)會去除二價陽離子(Mg2?、Ca2?),削弱 LPS 聚集體的鹽橋結構,降低其剛性;第二步,表面活性劑(如吐溫 20)嵌入 LPS 分子,形成混合聚集體(膠體、層狀結構),改變 LPS 的超分子形態。LPS 從 “可檢測態” 轉為 “不可檢測態”,導致鱟試劑中的 C 因子無法與內毒素結合,內毒素檢測出現假陰性。這種變化是時間依賴的,與稀釋度無關,給常規內毒素檢測帶來獨特挑戰。 鱟試劑靈敏度復核至關重要,存放半年需重測,避免內毒素檢測出現假陰性或假陽性。江...
2025-09-29 -
 重組蛋白內毒素檢測凝膠法鱟試劑
重組蛋白內毒素檢測凝膠法鱟試劑內毒素檢測結果誤差可能源于多環節:試劑方面,鱟試劑(LAL )或試劑批間差異、過期試劑活性下降會導致結果偏差,需通過試劑驗收(如陽性對照回收率驗證)確保質量;操作方面,實驗器具未除熱原(如玻璃器皿未干熱滅菌)、加樣體積不準確會引入污染或誤差,需嚴格執行 SOP(如器皿 250℃干熱滅菌≥30 分鐘);環境方面,實驗室空氣中的微生物孢子、粉塵可能污染樣品,需在潔凈工作臺操作并設置陰性對照。此外,反應溫度波動(偏離 37℃±1℃)會影響酶活性,需使用恒溫孵育器精確控溫,確保反應條件穩定。 內毒素檢測中,脂多糖(LPS) 聚集體過度變小(近單體)可能降低檢測信號。重組蛋白內毒素檢測凝膠法鱟試劑 ...
2025-09-29 -
 上海血液制品內毒素檢測重組級聯試劑(rCR)
上海血液制品內毒素檢測重組級聯試劑(rCR)重組級聯試劑作為內毒素檢測鱟試劑的理想替代方案,其具備的優勢有:①優化的G因子級聯反應,無G因子旁路干擾。采用基因重組技術表達鱟血細胞中的C因子(Factor C)、B因子(Factor B)和凝固酶原(Proclotting enzyme),無G因子旁路干擾,排除1,3-β-D葡聚糖假陽性風險。②依然采用動態顯色法原理,可沿用天然鱟試劑檢測設備。重組級聯試劑(rCR),與天然鱟(動態顯色法)具有相同的操作流程、檢測設備、分析方法,用戶可以沿用天然鱟的儀器、軟件、耗材、人員培訓、驗收程序等,無需投入額外成本。③具有與天然鱟的相同反應機制,檢測結果具有等效性。完全模擬了天然鱟試劑的酶聯反應,...
2025-09-28 -
 內毒素檢測方法驗證
內毒素檢測方法驗證內毒素檢測的實驗方案需遵循“標曲可靠性驗證(靈敏度復核)-稀釋倍數計算-干擾試驗”的完整流程,以保障檢測結果準確合規。首先進行標曲可靠性試驗,用標準內毒素制備至少3個濃度的稀釋液(相鄰濃度間稀釋倍數不超過10,下限濃度不低于鱟試劑標示檢測限),每濃度設 3 支平行管,同時做2支陰性對照;當陰性對照的吸光度小于或透光率大于標準曲線下限的檢測值或反應時間大于標準曲線下限的反應時間,對數據進行線性回歸,相關系數r的幅值≥0.980時試驗方有效,否則需重新操作。接著按公式 L=K/M 確定樣本內毒素限值,K 值依給藥途徑而定,M結合人均60kg體重、1.62m2 體表面積及上限給藥劑量計算,也可參...
2025-09-28 -
 江蘇醫療器械內毒素檢測抗干擾方案
江蘇醫療器械內毒素檢測抗干擾方案湖州申科生物凝膠法鱟試劑憑借合規性和實用性,成為實驗室內毒素定量檢測的優先選擇。該產品嚴格符合 USP、EP、中國藥典標準,提供 0.03、0.06、0.125、0.25、0.5EU/mL 等多種靈敏度規格,適配不同樣品的限值要求。設計上采用大瓶裝量(10 反應 / 支),減少瓶間差異和頻繁開瓶導致的污染風險,降低單位測試成本。針對血源制品、中藥注射劑等復雜基質樣品,配套特異性抗增液(NND071)可高效抑制非特異性反應,減少假陽性結果。包裝選用易開啟西林瓶,避免操作時玻璃碎屑污染,提升使用安全性。憑借千家醫院的臨床使用經驗和穩定的性能表現,該產品更適合血源制品及復雜基質。 凝膠法鱟試劑通...
2025-09-28 -
 廣東化學制藥內毒素檢測商業化試劑盒
廣東化學制藥內毒素檢測商業化試劑盒在進行內毒素檢測時,干擾試驗又叫增強或抑制試驗,主要目的是確證檢測內毒素的方法是否受樣品干擾。在建立細菌內毒素檢查方法中,驗證試驗前,要去除樣品可能含有的內毒素,以確保建立方法的準確可靠。藥典規定:①當進行新藥的內毒素檢查試驗前,或無內毒素檢查項品種建立內毒素檢查法時,需進行干擾試驗;②當鱟試劑、供試品的配方、生產工藝改變,或試驗環境下發生了任何有可能影響試驗結果的變化時,需重新進行干擾試驗。生產廠家常發生的一些微小變更,會影響到評估結果,進而影響到供試品對鱟試劑的干擾試驗。因此,生產廠家應制定一個重復進行干擾試驗的周期,并進行跟蹤和記錄。 內毒素檢測凝膠法實驗需西林瓶等耗材,確保無外源內...
2025-09-28 -
 上海高效內毒素檢測法規要求
上海高效內毒素檢測法規要求檢測細菌內毒素的堂試劑方法,是一個生物反應過程,受到很多因素的干擾。在一個供試品的檢測方法固定下來之前,為了得到準確的結果,必須要了解供試品與鱟試劑之間的相互關系。供試品中的成分往往非常復雜,而且會干擾試驗檢測系統的功能。很多干擾的機理,并不是非常清楚。但是業界比較能夠接受的理論是,如果供試品中某些因子影響了鱟試劑中蛋白的表達功能,則被認為是干擾作用(Inhibition/Enhancement,V/E)。干擾作用產生的因素較多,一般包括試劑因素(鱟試劑、內毒素標準品)供試品因素(pH值、溫度、離子強度、濃度、水溶性、黏度、可發生鱟試劑反應的非內毒素雜質)和實驗因素(試驗器皿、細菌內毒素檢...
2025-09-28 -
 江蘇生物制品內毒素檢測商業化試劑盒
江蘇生物制品內毒素檢測商業化試劑盒內毒素檢測常與熱原檢測混淆,二者既有關聯又有區別:熱原是指所有能引起發熱的物質(包括內毒素、病毒、真菌等),通過傳統家兔熱原試驗檢測;內毒素是熱原的主要成分(占 90% 以上),檢測更具特異性。目前,家兔熱原試驗因操作復雜、動物成本高,已逐漸被單核細胞活化反應測定法(MAT)替代,但部分產品(如放射性質藥物、血液制品)仍需保留家兔試驗作為補充。法規要求內毒素檢測結果需與熱原風險關聯,若內毒素檢測合格但臨床出現熱原反應,需排查是否存在非內毒素類熱原,通過聯合檢測確保產品安全性。 針對特殊樣本,rCR 在細菌內毒素檢測中的不干擾稀釋倍數(NID)比重組C因子(rFC)更低。江蘇生物制品內毒素檢...
2025-09-28 -
 上海合規性內毒素檢測
上海合規性內毒素檢測在為新物料或新產品、中間產品建立細菌內毒素檢測方法時,常會遇到各種困難,尤其是尚處于新藥研發早期階段的藥物。此時,由于藥物制劑、緩沖系統等還不穩定,經常會發生變化,這樣就給方法的建立帶來了不同程度的影響。在建立細菌內毒素檢查法之前,須盡可能多地了解有關該藥品的基本信息,例如:有關樣品的可溶性信息、推薦的稀釋液、在水中的溶解度以及合適溶劑,樣品的pH范圍,分子量大小;如果是蛋白產品,還要了解該產品的等電點,產品規格、體積或重量,擬用于臨床的用法和用量等,以便選擇合適的樣品處理方法和內毒素檢測方法。 細菌內毒素試驗(BET)是用鱟變形細胞裂解物(LAL)測內毒素的體外方法,LAL 測試獲國際藥...
2025-09-28